국산 및 외국산 벌꿀에서 6종의 네오니코티노이드계 농약 잔류조사
Abstract
In the present study, we determined six neonicotinoid (acetamiprid, clothianidin, dinotefuran, imidacloprid, thiacloprid, thiamethoxam) residues in 30 kinds of honey originated from Republic of Korea and different countries using HPLC-MS/MS. As a result of analyzing 6 types of neonicotinoid pesticides in 30 honey samples produced in Korea and foreign countries, all neonicotinoid insecticides were not detected in 28 of the 30 samples. In one sample from New Zealand (Manuka tree), dinotefuran was detected below the limit of quantitation, and in one sample from Korea (apple tree), acetamiprid was detected above the limit of quantification, at 176 ppb, which is above the residue limit set by the European Union. The six types of neonicotinoids examined were not detected in honey samples from 10 countries (United States, Italy, Mexico, Greece, Russia, Turkmenistan, Germany, Thailand, Uzbekistan, and Vietnam). In Korea, acetamiprid is a moderately toxic substance (class 3) to humans and livestock and is used in combination with other pesticide ingredients to control aphids and moths in apples, pears, and peaches, even before harvest. Therefore, it is believed that acetamiprid remains in apple honey because pesticides containing acetamiprid were used to control aphids during the flowering period of apple trees, and the honey was contaminated as bees engaged in foraging activities during this period. The study suggests that the use of neonicotinoid pesticides during the flowering season of fruit trees could contaminate honey with these pesticides and more extensive residue surveys are needed for fruit honey produced in this way.
Keywords:
Honey, Neonicotinoid insecticides, Residues, Monitoring, LC-MS/MS서 론
네오니코티노이드계 농약은 1990년대에 처음으로 사용이 되기 시작하여 광범위한 작물에 살충제로서 사용되고 있다 (Wood and Goulson, 2017). 야채류, 곡물, 콩류, 과일, 채소, 관상식물 등 다양한 농작물에 대해 씨앗 코팅, 토양 적용, 잎 표면 살포의 형태로 사용이 승인되어 있다 (Codling et al., 2016). 네오니코티노이드계 살충성분은 곤충의 중추신경계에 위치한 신경 시냅스에서 막의 탈분극과 관련된 니코틴성 아세틸콜린 수용체 (nAChR)에 작용하여 독성을 일으킨다. 네오니코티노이드 살충제는 포유류의 nAChR에 비해 곤충의 nAChR에 대한 친화성이 높아, 포유동물에 상대적으로 독성이 낮은 선택성이 높은 살충제이다 (Gbylik-Sikorska et al., 2015). 이러한 장점으로 식물에서 진딧물 등을 구제하기 위한 살충제로서 매우 많이 사용되어져 왔지만, 최근에는 수분 매개자인 꿀벌에게는 치명적인 독성이 있는 것으로 보고되고 있다 (Jones and Turnbull, 2016). 특히, 북미와 유럽에서 호박벌 감소의 원인으로 의심되고 있다 (Christopher Cutler and Scott-Dupree, 2014).
네오니코티노이드는 식물에 흡수되어 꽃을 포함한 모든 기관으로 이동하여 꽃가루, 꽃꿀은 물론 식물에서 생산되는 모든 생산물에 잔류될 수 있다. 꽃꿀과 꽃가루의 농약오염은 꿀벌에서 직접적인 독성으로 이어지고, 심지어는 꿀에 오염된다 (Jones and Turnbull, 2016). 꿀벌은 생존을 위해 꽃꿀과 꽃가루에 의존하며, 벌집에서 최대 4 km 또는 그 이상 떨어진 곳까지 이동하여 꽃꿀과 꽃가루를 수확할 수 있다 (Gaweł et al., 2019). 꿀벌의 이러한 특성을 고려하면 벌집에서 나온 꿀에서의 살충제 잔류 수준은 주변 환경의 오염을 측정하는 기준이 될 수 있는 것으로 알려져 있다 (Ligor et al., 2020).
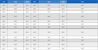
꿀은 항균, 항진균, 항결핵, 항바이러스와 같은 광범위한 효과를 보인다 (Israili, 2014). 그러나, 꿀벌의 네오니코티노이드 노출은 꿀의 오염으로 이어지며 인간 건강에 대한 잠재적 위험을 유발할 수 있다 (Gbylik-Sikorska et al., 2015). 네오니코티노이드는 기존 살충제에 비해 포유류에게 독성이 낮은 것으로 간주되지만, 점점 더 많은 연구에서 네오니코티노이드에 노출되면 포유류에게 잠재적인 위험이 있음을 보여준다. 노출 시 생식독성, 간독성, 신경독성, 유전독성 등을 일으켜 인간에게 치명적인 독성을 일으킬 수도 있다 (Han et al., 2018). 이러한 네오니코티노이드계 농약의 잠재적 위험에서 국민을 보호하기 위해 유럽연합 (EU)에서는 꿀에 네오니코티노이드계 살충성분의 잔류허용기준을 10~200 μg/kg으로 설정하고 있다 (Table 1).
지금까지 꿀에 잔류하는 네오니코티노이드계 살충제를 조사하는 다수의 연구 결과들이 보고되었다. Mrzlikar 등은 LC-MS/MS를 이용하여 슬로베니아에서 생산된 51개의 꿀에서 네오니코티노이드를 조사하였으며 (Mrzlikar et al., 2019), Tanner 등은 LC-MS/MS를 이용하여 오스트리아에서 생산된 41개의 꿀에서 네오니코티노이드계 살충제 및 2가지 대사산물을 조사하였다 (Tanner and Czerwenka, 2011). Jones 등은 LC-MS/MS를 이용하여 영국에서 생산된 22개의 꿀에서 네오니코티노이드를 조사하였으며 (Jones and Turnbull, 2016), Gaweł 등은 LC-MS/MS를 이용하여 폴란드에서 생산된 155개의 꿀에서 네오니코티노이드 및 199가지 살충제를 조사한 결과를 보고한 바 있다 (Gaweł et al., 2019). 꿀 이외에 시료에서 네오니코티노이드 잔류수준에 대한 조사 연구도 수행되었는 바, Kim 등은 HPLC를 이용하여 한국의 음용수 처리장에서 네오니코티노이드 농도 분포를 조사하였고 (Kim et al., 2021), Park 등은 UPLC를 이용하여 한국의 과일 및 채소에서 네오니코티노이드계 농약을 모니터링하였다 (Park et al., 2010).
본 연구자들이 조사한 결과로는 현재까지 국내에서는 꿀에서 네오니코티노이드를 조사한 결과를 확인할 수 없었다. 따라서 본 연구에서는 꿀에서 잔류가능성이 있는 6종의 네오니코티노이드계 살충제 (acetamiprid, clothianidin, dinotefuran, imidacloprid, thiacloprid, thiamethoxam)를 분리 정제하여 LC-MS/MS로 동시에 정량 분석하는 방법을 활용하여 국내와 외국에서 생산된 30개의 꿀에서 6종의 네오니코티노이드계 살충성분의 잔류수준을 조사하였다.
재료 및 방법
1. 시약 및 기기
표준물질 acetamiprid, clothianidin, dinotefuran, imidacloprid, thiacloprid, thiamethoxam은 모두 Sigma-Aldrich사 (Gangnam-gu, Seoul, Republic of Korea)에서 구입하였고, 시험에 사용된 sodium phosphate monobasic, MgSO4, NaCl은 Sigma-Aldrich사에서 구입하였으며, dispersive kit는 Agilent사의 5982-4950을 사용하였다. LC-MS/MS 분석에 사용한 모든 용매는 HPLC 등급을 사용하였고, 0.1% formic acid in water, 0.1% formic acid in acetonitrile는 Fisher chemical사, acetonitrile은 Sigma-Aldrich사 제품을 사용하였다. 3차 증류수는 Water purification system (EXL 7 Bio)을 이용하여 제조하였다. 교반기는 MaXshake (Daihan, Wonju, Republic of Korea)을 사용하였고, 다중튜브교반기는 LM-2500 (SHsigma, Suwon, Republic of Korea)을 사용하였다. 원심분리기는 Eppendorf 5804R (Eppendorf, Hamburg, Germany)을 사용하였다. 질소농축기는 Evatros T.C.S (Goojung EnT, Seoul, Republic of Korea)를 사용하였다. 액체 크로마토그래피-질량분석기 (liquid chromatography-mass spectrometry, LC-MS/MS)는 LCMS-8050 (Shimadzu, Kyoto, Japan)을 사용하였다. LC-MS/MS에는 system controller (SCL-40), binary pump (LC-40B X3), autosampler (SIL-40C X3), column oven (CTO-40S)으로 구성되었다. 분석용 칼럼은 Sunfire C18 (2.1×150 mm, 3.5 μm)을 사용하였으며 Waters (Milford, Massachusetts, United States)에서 구입하였다.
2. 시료 수집
다양한 밀원에서 유래한 (아카시나무, 벚나무, 헛개나무, 감나무 등) 30개의 꿀 시료는 국내 및 다른 여러 국가 (미국, 이탈리아, 멕시코, 그리스, 러시아, 튀르키예, 뉴질랜드, 독일, 태국, 우즈베키스탄, 베트남)에서 생산된 꿀을 구매하거나 직접 외국에서 수집하였다 (Table 2). 30개의 꿀 중에서 국산 꿀 (13종)과 미국 (3종), 이탈리아 (3종), 멕시코 (2종), 그리스 (2종), 러시아 (1종), 튀르키예 (1종), 뉴질랜드 (1종), 독일 (1종), 태국 (1종), 우즈베키스탄 (1종), 베트남 (1종)으로 구성되었다. 밀원은 제품의 표시사항으로 결정하였으며 별도의 밀원 확인 과정을 거치지 않았다. 모든 시료는 실온에서 차광하여 보관하였다.
3. 표준용액의 제조
표준원액은 각 표준품의 순도를 고려하고 methanol 양을 조절하여 녹여 농도가 1,000 μg/mL이 되도록 조제하였다. 표준원액은 냉동 (-20℃) 보관하였다.
4. 기기분석 및 시료 전처리
액체 크로마토그래프 조건 및 질량분석기 조건, 시료 전처리 방법은 Nam 등의 조건을 이용하였다 (Nam et al., 2024).
결과 및 고찰
국내와 외국에서 생산된 30개의 꿀 시료에 대해서 6종의 네오니코티노이드계 살충성분의 잔류를 조사한 결과, 30개의 시료 중 28개에서는 조사한 모든 네오니코티노이드계 살충성분이 검출되지 않았으며 뉴질랜드 1개의 시료 (마누카나무 유래 꿀)에서 dinotefuran이 정량한계 미만으로 검출되었고, 대한민국 1개의 시료 (사과나무 유래 꿀)에서 acetamiprid가 정량한계 이상으로 유럽연합에서 설정한 잔류허용기준 이상인 176 ppb가 검출되었다 (Table 3). 10개의 나라 (미국, 이탈리아, 멕시코, 그리스, 러시아, 튀르키예, 독일, 태국, 우즈베키스탄, 베트남)의 꿀 시료에서는 조사한 6종의 네오니코티노이드계 살충성분이 검출되지 않았다. 사용한 분석법에서 6종의 네오니코티노이드계 살충성분에 대한 검출한계 (LOD)는 Table 3의 아래 주석과 같았다.
꿀벌은 생존하고 군집을 늘리기 위해서 꽃에서 화밀이나 화분을 영양분으로 사용하고 있어 꽃이 피는 시기에 화밀이나 화분에 농약 등이 오염될 수 있다. 이러한 농약의 오염은 농업 현장에서의 사용에 의해서나 잔디 관리, 가정, 정원, 지역 공원 등에서 살충제가 사용되는 다양한 원인에 의해서 발생될 수 있다고 보고하였다 (Kavanagh et al., 2021).
꿀에 잔류하는 네오니코티노이드계 살충성분을 조사하는 다른 연구 결과들을 보면 Kavanagh 등은 아일랜드 꿀 시료에서는 네오니코티노이드계 살충제를 조사한 결과 imidacloprid (13.43%)가 가장 높게 검출되는 네오니코티노이드이었으며, clothianidin (12.40%)과 thiacloprid (11.37%)가 그 뒤를 이었다고 보고하였다 (Kavanagh et al., 2021). Tanner 등은 오스트리아 꿀 시료에서 acetamiprid, thiacloprid, thiamethoxam이 검출되었으나 0.6~5 μg/kg 및 2~10 μg/kg의 낮은 검출 및 정량 한계로 잔류허용기준을 초과한 시료는 없었다 (Tanner and Czerwenka, 2011). Ligor 등은 폴란드 및 기타 국가의 꿀 시료 53개를 분석한 결과, 그리스 (1개 시료), 카메룬 (1개 시료), 호주 (3개 시료), 브라질 (1개 시료), 이탈리아 (1개 시료), 폴란드 (12개 시료)의 꿀 시료 19개에서 네오니코티노이드가 정량한계보다 높은 농도로 검출되었다고 보고하였다 (Ligor et al., 2020). 본 연구에서 대한민국 및 미국, 이탈리아, 멕시코, 그리스, 러시아, 튀르키예, 뉴질랜드, 독일, 태국, 우즈베키스탄, 베트남 등에 생산된 꿀 시료 30개에서 6종의 네오티코티노이드계 살충성분을 잔류조사한 결과, 대한민국 (1개 시료), 뉴질랜드 (1개 시료)를 제외하고 모든 검사시료에서 불검출되었다. 검출된 물질은 acetamiprid, dinotefuran 이다.
국내에서는 네오니코티노이드계 살충성분 6종 (acetamiprid, clothianidin, dinotefuran, imidacloprid, thiacloprid, thiamethoxam)이 허가되어 있지만, 그중 꿀벌에 위해성이 높다고 추정되는 imidacloprid, clothianidin, thiamethoxam, dinotefuran 4종에 대해서 꽃이 피어 있는 시기에는 사용을 금지하고 있다 (Rural Development Administration, Agrochemical Safety Information System, 2025). Dinotefuran은 일벌의 학습능력, 채밀 능력에 영향을 미치는 것으로 알려져 있다 (Liu et al., 2019). 본 연구에서는 뉴질랜드 마누카꿀에서 정량한계 이하의 dinotefuran이 검출되어 이들 농약이 채밀기에 벌들에게 노출될 수 있음을 시사하고 있다. 본 연구에서 잔류허용기준보다 높은 농도로 검출된 꿀의 밀원은 사과나무이다. 과일나무는 상업적 농업 환경에서 재배되기 때문에 생산량 증대를 위해 해충 방제를 위한 농약을 자주 사용하지만, 야생 밀원 식물의 경우에는 농약 살포가 적거나 없는 지역에서 자라므로 꿀벌이 채밀하는 동안 농약 노출이 상대적으로 적을 수 있어 과실에서 채집한 꿀에는 농약이 더 많이 검출될 가능성이 높을 것으로 판단된다.
국내에서 생산된 사과꿀 1개에서 acetamiprid가 유럽의 잔류허용기준을 초과하였다. 우리나라에서 acetamiprid는 사람과 가축에서 3급의 보통독성 물질로서 다른 농약성분들과 합제로 사과, 배, 복숭아 등의 진딧물이나 나방 등을 방제할 목적으로 수확기전까지 사용하도록 되어 있다. 따라서 사과의 개화기에 진딧물 등을 구제할 목적으로 acetamiprid가 포함된 살충제를 사용하였고 이 시기에 꿀벌들이 채밀 활동을 함으로써 꿀에 이 농약성분이 오염되었을 것으로 추정된다.
네오니코티노이드계 살충성분이 사람에게 미치는 영향을 조사한 연구 결과들을 보면 태반의 영양막 세포에 acetamiprid 상용 제형을 24시간 동안 노출시킨 결과, 분석된 모든 농도 (0.1, 1, 10, 100 μM)에서 세포 생존율을 유의 미하게 감소시키고, ROS 생성을 유발하였다고 보고하였다 (Gomez et al., 2020). 배아 세포의 다양한 네오니코티노 이드에 대한 민감도는 thiacloprid>acetamiprid, thiamethoxam>clothianidin 순으로서 사람에서는 오히려 꿀벌에 위해성이 높다고 추정되는 clothianidin보다 thiacloprid와 acetamiprid가 상대적으로 위해성이 높다고 보고되어 있다 (Babel’ová et al., 2017). 본 연구에서는 사과꿀에서 acetamiprid가 176 ng/mL로 검출되었다. 이러한 오염수준은 유럽의 잔류허용기준의 3.5배에 해당되며, 이 성분이 사람에게서 상대적 위해성이 높다는 점과 꿀의 다소비층을 고려할 때 향후 과실나무 유래 꿀에서의 이들 성분에 대한 광범위한 잔류조사와 잔류조사 결과들을 활용한 공중보건학적 관점에서의 노출평가가 필요할 것으로 사료 된다.
Acknowledgments
이 논문은 농림축산검역본부 (Z-1543073-2024-25-01)와 2024학년도 세명대학교 대학혁신지원사업의 지원을 받아 수행되었다. 실험을 도와준 오은서 학생에게 감사드립니다.
References
-
Babel’ová, J., Z. Šefčíková, Š. Čikoš, A. Špirková, V. Kovaříková, J. Koppel, A. V. Makarevich, P. Chrenek and D. Fabian. 2017. Exposure to neonicotinoid insecticides induces embryotoxicity in mice and rabbits. Toxicology 392: 71-80.
[https://doi.org/10.1016/j.tox.2017.10.011]

-
Christopher Cutler, G. and C. D. Scott-Dupree. 2014. A field study examining the effects of exposure to neonicotinoid seed-treated corn on commercial bumble bee colonies. Ecotoxicology 23(9): 1755-1763.
[https://doi.org/10.1007/s10646-014-1340-5]

-
Codling, G., Y. Al Naggar, J. P. Giesy and A. J. Robertson. 2016. Concentrations of neonicotinoid insecticides in honey, pollen and honeybees (Apis mellifera L.) in central Saskatchewan, Canada. Chemosphere 144: 2321-2328.
[https://doi.org/10.1016/j.chemosphere.2015.10.135]

-
Gaweł, M., T. Kiljanek, A. Niewiadowska, S. Semeniuk, M. Goliszek, O. Burek and A. Posyniak. 2019. Determination of neonicotinoids and 199 other pesticide residues in honey by liquid and gas chromatography coupled with tandem mass spectrometry. Food Chem. 282: 36-47.
[https://doi.org/10.1016/j.foodchem.2019.01.003]

-
Gbylik-Sikorska, M., T. Sniegocki and A. Posyniak. 2015. Determination of neonicotinoid insecticides and their metabolites in honeybees and honey by liquid chromatography tandem mass spectrometry. J. Chromatogr. B Analyt. Technol. Biomed. Life Sci. 990: 132-140.
[https://doi.org/10.1016/j.jchromb.2015.03.016]

-
Gomez, S. D., P. S. Bustos, V. G. Sánchez, M. G. Ortega and N. Guiñazú. 2020. Trophoblast toxicity of the neonicotinoid insecticide acetamiprid and an acetamiprid-based formulation. Toxicology 431(15): 152363.
[https://doi.org/10.1016/j.tox.2020.152363]

-
Han, W., Y. Tian and X. Shen. 2018. Human exposure to neonicotinoid insecticides and the evaluation of their potential toxicity: An overview. Chemosphere 192: 59-65.
[https://doi.org/10.1016/j.chemosphere.2017.10.149]

-
Israili, Z. H. 2014. Antimicrobial Properties of Honey. Am. J. Ther. 21(4): 304-323.
[https://doi.org/10.1097/MJT.0b013e318293b09b]

-
Jones, A. and G. Turnbull. 2016. Neonicotinoid concentrations in UK honey from 2013. Pest Manag. Sci. 72(10): 1897-1900.
[https://doi.org/10.1002/ps.4227]

-
Kavanagh, S., M. Henry, J. C. Stout and B. White. 2021. Neonicotinoid residues in honey from urban and rural environments. Environ. Sci. Pollut. Res. Int. 28(22): 28179-28190.
[https://doi.org/10.1007/s11356-021-12564-y]

-
Kim, J., W. Wang, S. Lee, J. H. Park and J. E. Oh. 2021. Concentrations and distributions of neonicotinoids in drinking water treatment plants in South Korea. Environ. Pollut. 288(1):117767.
[https://doi.org/10.1016/j.envpol.2021.117767]

-
Ligor, M., M. Bukowska, I. A. Ratiu, R. Gadzała-Kopciuch and B. Buszewski. 2020. Determination of Neonicotinoids in Honey Samples Originated from Poland and Other World Countries. Molecules 25(24): 5817.
[https://doi.org/10.3390/molecules25245817]

-
Liu, S., Y. Liu, F. He, H. Zhang, X. Li and H. Tan. 2019. Enantioselective Olfactory Effects of the Neonicotinoid Dinotefuran on Honey Bees (Apis mellifera L.). J. Agric. Food Chem. 67(43):12105-12116.
[https://doi.org/10.1021/acs.jafc.9b04851]

-
Mrzlikar, M., D. Heath, E. Heath, J. Markelj, A. Kandolf Borovšak and H. Prosen. 2019. Investigation of neonicotinoid pesticides in Slovenian honey by LC-MS/MS. LWT. 104: 45-52.
[https://doi.org/10.1016/j.lwt.2019.01.017]

-
Nam, S. M., J. H. Bae, D. H. Kim and H. G. Kang. 2024. Simultaneous residue analysis of neonicotinoid insecticides in honey using LC-MS/MS. J. Prev. Vet. Med. 48(4): 262-269.
[https://doi.org/10.13041/jpvm.2024.48.4.262]

- Park, B. J., K. A. Son, M. K. Paik, J. B. Kim, H. Y. Kwon, S. M. Hong, G. J. Im and M. K. Hong. 2010. Monitoring of Neonicotinoid Pesticide Residues in Fruit Vegetable and Human Exposure Assessment. Korean J. Pestic. Sci. 14(2): 104-109.
- Rural Development Administration. Agrochemical Safety Information System. 2025. https://psis.rda.go.kr/psis/index.ps, 13 Feb.2025.
-
Tanner, G. and C. Czerwenka. 2011. LC-MS/MS analysis of neonicotinoid insecticides in honey: Methodology and residue findings in Austrian honeys. J. Agric. Food Chem. 59(23): 12271-12277.
[https://doi.org/10.1021/jf202775m]

-
Wood, T. J. and D. Goulson. 2017. The environmental risks of neonicotinoid pesticides: a review of the evidence post 2013. Environ. Sci. Pollut. Res. Int. 24(21): 17285-17325.
[https://doi.org/10.1007/s11356-017-9240-x]