국내 꿀벌 (Apis mellifera) 유전자원에 대한 꿀벌응애 (Varroa destructor) 저항성 연관 유전자 발현 비교 분석
Abstract
The ectoparasitic mite Varroa destructor, which parasitizes honeybee fat body and transmits lethal viruses, is a major cause of overwinter colony losses. In addition to chemical treatment and management practices, the development of Varroa-resistant honeybee strains provides a sustainable strategy for effective control. To provide a foundation for resistance breeding, we investigated the expression of candidate resistance-related genes in honeybee strains, based on previous studies, The genes TANC2 and baz showed no significant expression differences between Varroa-free and infected pre-pupae but were upregulated in infected pupae. Comparative analysis across five honeybee strains (A, C, D, F, V) revealed that strains D and V exhibited significantly higher expression of Alh and hormone receptor 78, both associated with Varroa-resistance. Furthermore, analysis of nine Varroa-sensitive hygiene (VSH) genes and two olfactory genes in brain tissue revealed strain-specific variation, although consistent expression patterns were not evident across all genes. These findings demonstrate differential expression of Varroa-resistance related genes among honeybee strains and provide baseline information that may support the development of Varroa-resistant honeybee strains.
Keywords:
Apis mellifera, Varroa destructor, Varroa-sensitive hygiene, Resistant strains, Gene expression서 론
양봉꿀벌 (Apis mellifera)은 작물 화분매개를 통해 식량 생산에 기여하며 벌꿀, 로열젤리, 프로폴리스 등의 양봉산물을 생산하는 생태·경제적으로 매우 중요한 곤충이다 (Jung, 2008; Ruttner, 2013; Yoon et al., 2021; Minaud et al., 2024). 최근 전 세계적으로 일어나는 월동폐사로 인한 꿀벌 집단소실은 식량안보와 양봉산업 전반에 위협을 가하고 있다 (Kim and Lee, 2022; Minaud et al., 2024). 월동폐사는 한 가지 요인이 아닌 여러 가지 요인들이 복합적으로 작용하여 일어난다 (Highfield et al., 2009; Desai and Currie, 2016; Requier et al., 2019; Insolia et al., 2022). 주요 요인으로 꿀벌 기생성 응애류가 있다 (Cox-Foster et al., 2007; Guzmán-Novoa et al., 2010; Kim, 2022). 꿀벌 기생성 응애류는 내부기생성인 기문응애 (Acarapis woodi), 외부기생성인 꿀벌응애 (Varroa destructor)와 중국가시응애 (Tropilaelaps mercedesae)로 구분할 수 있다. 우리나라는 꿀벌응애 (V. destructor)와 중국가시응애 (T. mercedesae)의 피해가 심각하며 기문응애 (A. woodi)는 현재 우리나라에서 존재가 확인되지 않았다 (Choi et al., 2014; Kim et al., 2019). 꿀벌응애는 기존에 동양종 꿀벌 (A. cerana)을 기주로 삼았으나, 양봉꿀벌이 도입되고 두 종의 서식처 간 경계가 붕괴되면서 양봉꿀벌로 기주 전환된 후 전 세계로 확산되었다 (Rinderer et al., 2001; Traynor et al., 2020; van Alphen and Fernhout, 2020; Grindrod and Martin, 2023). 이들이 꿀벌에 감염되면 산물 생산성 저해 및 질병 매개, 면역력 저하 등의 문제를 야기한다 (Shimanuki et al., 1994; Chen et al., 2006; Choi et al., 2014; Roth et al., 2020). 중국가시응애 (T. mercedesae)는 Delfinado와 Baker에 의해 1961년에 최초로 보고되었으며 꿀벌응애 (V. destructor)보다도 봉군에 많은 피해를 입힐 수 있다 (Burgett and Akratanakul, 1983; Choi et al., 2014; Kang et al., 2024; Oh et al., 2024). 중국가시응애와 꿀벌응애는 꿀벌에 치명적인 날개불구바이러스 (deformed wing virus; DWV), 급성꿀벌마비바이러스 (acute bee paralysis virus) 및 이스라엘급성마비바이러스 (israeli acute paralysis virus) 등을 매개한다 (Govan et al., 2000; Gisder et al., 2009; Chen et al., 2014). 꿀벌응애는 꿀벌의 면역 경로를 억제함으로써 바이러스들의 증식에 간접적으로 기여해 꿀벌 집단폐사에 영향을 미친다 (Bailey et al., 1963; Lanzi et al., 2006; Berthoud, 2010; Weaver et al., 2021). 이에 우리나라에서 발생하는 월동폐사의 주 원인으로 꿀벌응애가 지목되었다 (Kim, 2022; Truong et al., 2022). 꿀벌응애로 인한 월동폐사 대응책으로 선제적 방제가 강조되고 있으나, 최근 국내 연구 결과 플루발리네이트 (fluvalinate)와 아미트라즈 (amitraz) 등과 같은 화학적 방제제에 저항성을 가지는 꿀벌응애 발생이 보고되었다 (Kim and Lee, 2022; Lee et al., 2023, 2025).
꿀벌응애류 방제에서 화학적 약제의 효과가 점차 제한됨에 따라 꿀벌응애 저항성 품종 개발 시도가 이루어지고 있다. 꿀벌의 응애 저항성은 성충 일벌의 Varroa-sensitive hygiene (VSH)에 의한 행동 저항성과 번데기에서 유전자 발현 조절을 통해 감염에 대응하는 생리적 저항성으로 구분된다 (Navajas et al., 2008; Le Conte et al., 2011; Conlon et al., 2019). 저항성 품종 육성을 위해서는 위 두 가지 특성 모두를 확보하는 것이 중요하다. Büchler et al. (2020)은 위생행동 및 몸단정행동 등을 종합하여 꿀벌응애 저항성 형질을 평가하였다. 이를 활용해 선발육종으로 개발된 미국의 Pol-line 품종은 DWV의 감염 전파율까지 낮추는 효과가 보고되었으나 (Danka et al., 2016; O’Shea-Wheller et al., 2022), 본 품종은 잡종강세 육종 기술을 적용하여 F1 세대에서 강한 저항성을 보이더라도 세대를 거듭할수록 그 특성이 약화되는 단점을 가진다. 유전자 수준에서 꿀벌응애 저항성 기작을 이해하기 위한 다양한 연구가 수행되었다. 위생행동 빈도에 차이를 보이는 꿀벌계통의 전사체 분석을 통해 면역 (defensin, hymenoptaecin), 후각 및 신경기능 (odorant receptors, neuroligin, GABA receptor), 행동 조절 (myosin 20, ataxin-2) 관련 유전자들의 차등 발현이 꿀벌응애 저항성과 연관될 수 있음을 보였다 (Navajas et al., 2008; Le Conte et al., 2011; Boutin et al., 2015). 응애 감염 시 꿀벌의 자가 몸단정행동 강도에 따라 차등 발현되는 neurexin-1 (AmNrx1), poly-U binding factor 68, cytochrome P450 등의 유전자 중 AmNrx1은 몸단정행동과 가장 강하게 연관된 지표 유전자로 보고되었다 (Hamiduzzaman et al., 2017). 꿀벌의 위생행동은 과거 번데기 덮개 제거 (uncapping)와 감염되거나 죽은 유충 또는 번데기를 제거 (removal)하는 두 개의 단일 유전자에 의해 조절된다고 알려졌다 (Rothenbuhler, 1964). 추후 연구에서는 uncapping과 removal은 서로 다른 양적형질 유전좌위 (quantitative trait loci; QTL)에 의해 분리 조절되는 양적형질임이 확인되었다 (Lapidge et al., 2002). Oxley et al. (2010)은 hygiene (Hyg1, Hyg2, Hyg3), uncapping (Uncap1, Uncap2), 그리고 removal 1 (Rem1)의 6개 QTL 영역이 위생행동 개시를 위한 반응 임계값 (task threshold)에 영향을 준다고 보고하였다. 현재 꿀벌응애 저항성 기작을 규명하기 위해 수행되고 있는 다양한 연구는 마커 보조 선발을 통한 꿀벌응애 저항성 품종 육성에 핵심적인 기반이 된다. 국내에서도 꿀벌응애로 인한 월동피해 사례가 다수 보고되고 있는 만큼 우리나라에서도 꿀벌응애 저항성 품종 육성을 통해 근본적인 해결 방안을 마련해야 한다.
본 연구에서는 국내 양봉꿀벌을 대상으로 유전자 분석을 수행하여 향후 꿀벌응애 저항성 품종 육성을 위한 기반을 마련하고자 하였다. 국외 연구 결과를 참조하여 15개 후보 유전자를 선발하였다. 꿀벌응애 감염 유무에 따른 유전자 발현 차이는 비계통 양봉꿀벌의 전용유충과 번데기에서 조사하였다. VSH를 포함한 꿀벌응애 저항성 연관 유전자는 5계통의 양봉꿀벌 (A, C, D, F, V) 일벌 번데기와 뇌에서 그 발현을 비교 분석하였다.
재료 및 방법
1. 공시충 및 시료 채취
실험에 사용한 양봉꿀벌 (A. mellifera)은 꿀벌위도격리육종장 (전라북도 부안군 위도면, GPS: 35.591300, 126.279048)에서 관리중인 꿀벌을 사용하였다. 꿀벌응애 감염 유무에 따른 유전자 발현 조사는 비계통 양봉꿀벌을 사용해 수행되었다. 실험에는 3개 봉군을 사용하였다. 꿀벌 시료는 각 봉군으로부터 3마리씩 채집하였으며 이를 3회 반복하였다. 시료는 수벌과 일벌로 나누어 채집하였다. 번데기 덮개를 제거하여 벌집으로부터 전용유충과 번데기를 적출한 뒤 육안으로 확인하여 응애 감염/미감염을 분류하였다. 수벌은 봉개 후 24시간이 경과한 전용유충과, 용화 후 약 3일이 경과해 눈이 분홍색이 되는 시점의 번데기를 채집하였다. 일벌은 수벌과 같은 조건으로 번데기만을 채집하였다. 채집된 전용유충과 번데기는 충체 전부를 RNA 분리에 사용하였다.
꿀벌응애 저항성 연관 유전자 분석을 위해 사용된 꿀벌 유전자원은 표로 나타내었다 (Table 1). 실험 계통은 A, F계통 2봉군, C, D 3봉군, V 1봉군을 사용하였다. 꿀벌 시료는 빈 벌집에 마킹 후 해당 벌집에 여왕벌이 새로 산란한 알로부터 부화한 개체만을 채집하였다. 일벌 번데기는 앞서 언급한 내용대로 채집하였다. 일벌 성충은 각 봉군으로부터 우화 후 7일 이상 경과한 내역봉 10마리씩 3회 반복실험이 가능하도록 채집하였다. 성충은 머리를 해부한 뒤 뇌조직만을 채취하였다. 모든 해부 과정은 얼음 위에서 수행하였다. 해부된 꿀벌의 뇌는 Leica microscope MSV266 (Leica, Wetzlar, Germany)로 확인하였으며 Tucsen Mosaic 2.2.1 Software (Tucsen, Fuzhou, Fujian Province, China)를 사용해 촬영하였다. 채취된 시료는 즉시 RNA 분리를 위해 사용되었다.
2. RNA 분리 및 cDNA 합성
채취한 시료로부터 TRIzol® Reagent (Invitrogen, Carlsbad, CA, USA) 시약을 사용하여 제조업체의 지침에 따라 총 RNA를 분리하였다. 분리된 RNA의 농도 및 순도는 VivaSpec Spectrophotometer (Sartorius, Göttingen, Germany)를 사용해 측정하였다. 이후 cDNA 합성을 위해 RNA to cDNA EcoDryTM Premix (Oligo dT) (TaKaRa Bio, Shiga, Japan)와 함께 1 μg의 RNA를 사용하였다. PCR 조건은 42°C; 1시간, 70°C; 10분으로 수행하였다.
3. 실시간 중합효소 연쇄반응 (quantitative polymerase chain reaction; qPCR)
선발한 유전자에 대한 mRNA 발현 수준을 조사하기 위해 qPCR을 수행하였다. qPCR은 QuantStudioTM 5 Real-Time PCR System (Thermo Fisher Scientific, Madison, WI, USA)를 사용해 수행되었다. qPCR 반응은 TOPrealTM SYBR Green qPCR PreMIX (Enzynomics Inc, Daejeon, Republic of Korea)와 함께 80 ng의 cDNA와 5 pmol의 프라이머를 사용하여 최종적으로 20 μL 용량으로 진행하였다. 참조 유전자로는 actin을 사용하였다. 실험에 사용된 프라이머는 Table 2에 나타내었다. qPCR은 50°C; 2분, 95°C; 10분의 hold stage, 95°C; 15초, 60°C; 1분의 PCR stage를 40회 반복 후 마지막으로 95°C; 15초, 60°C; 1분, 95°C; 1분의 melt curve stage로 수행하였다.
4. 통계분석
통계분석은 R studio를 사용하여 수행하였다. 정규분포를 따르고 등분산성을 만족하는 두 개의 그룹을 비교하기 위해 t-test를 수행하였다. 3개 이상의 그룹을 비교할 때 정규분포를 따르고 등분산성을 만족할 경우 One-Way ANOVA test를 수행하였으며 이후 Tukey’s HSD로 유의성을 검정하였다. 만족하지 않는 경우 Kruskal-Wallis test를 수행하였으며 이후 Dunn’s test를 통해 유의성을 검정하였다.
결과 및 고찰
1. 꿀벌응애 (Varroa destructor) 감염에 반응하는 유전자 발현 분석
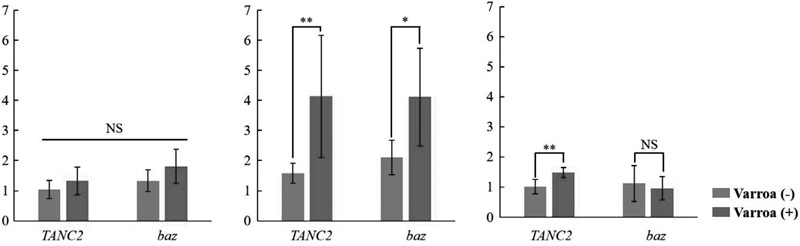
TANC2와 baz 유전자는 꿀벌응애 감염 번데기에서 발현이 증가하는 것으로 알려졌다 (Navajas et al., 2008). 수벌 전용유충과 번데기에서 감염 유무에 따른 두 유전자의 발현을 비교한 결과 전용유충에서는 응애 감염 시 발현 수준이 증가하는 경향을 보였으나 통계적으로 유의한 차이는 나타나지 않았다 (Fig. 1a). 번데기에서 응애 감염 시 두 유전자의 발현이 크게 증가하였다 (Fig. 1b). 일벌의 경우 응애 감염 번데기에서 TANC2의 발현 증가를 확인하였으나 baz는 유의미한 발현 차이를 보이지 않았다 (Fig. 1c). Boot et al. (1992)의 연구에 따르면 수벌의 경우 번데기 덮개가 덮이기 40~50시간 전, 일벌의 경우 15~20시간 전으로 꿀벌응애의 침입 시점이 다르다는 것이 밝혀졌다. 이는 수벌이 일벌보다 더 오랜 기간 꿀벌응애의 가해를 받는다는 점을 보여준다. 감염된 일벌 번데기가 보인 상대적으로 약한 발현양상은 응애 침입 및 가해 시점이 늦어 제한적인 발현 반응을 보인 것으로 판단된다. TANC2는 초파리 (Drosophila melanogaster)에서 발견된 CG9520과 상동 유전자로 보고되었다 (Navajas et al., 2008). CG9520은 초파리에서 GalNAcα-Ser/Thr (Tn 항원)으로부터 T 항원의 합성에 관여하는 것으로 알려져 있으며 신경계 형성과 혈액세포의 조절 및 배아 발달에 관여한다 (Yoshida et al., 2008). 해당 유전자의 돌연변이는 배아 치사와 혈구세포의 감소 및 신경계 형태이상을 유발한다 (Yoshida et al., 2008; Zhang and Ten Hagen, 2019). baz 또한 초파리의 날개와 눈 조직 발생 과정에서 notch 신호 전달 및 그에 따른 전사 활성화에 필수적이라는 것이 밝혀졌다 (Wu et al., 2024). 꿀벌응애 감염은 꿀벌의 면역능력을 감소시킬 뿐 아니라 DWV의 병원성 증가를 야기한다 (Martin et al., 2012; Ryabov et al., 2014; Weaver et al., 2021). DWV는 유충 또는 번데기 시기 날개원기 형성에 관여하는 유전자군의 발현에 변화를 일으키면서 기형을 유도한다 (Gisder et al., 2009; Ryabov et al., 2014). 초파리에서 알려진 기능과 꿀벌응애 감염 시 보인 발현 양상을 고려했을 때 DWV에 의한 배아발달 저해를 완화하기 위한 꿀벌의 방어 기작으로 발현된 것으로 판단된다.
2. 꿀벌응애 (Varroa destructor) 저항성 연관 유전자 분석
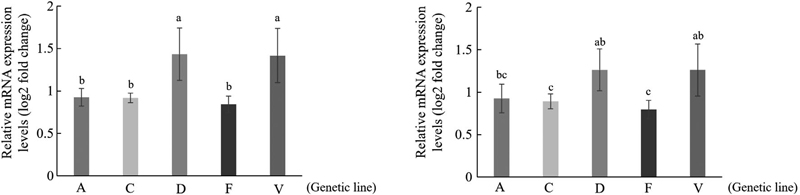
Navajas et al. (2008)은 꿀벌응애 저항성 품종에서 Alh와 Hormone receptor 78 (Hr78)의 발현이 상향조절된다고 밝혔으며, 각 계통별 꿀벌응애 저항성 기준 유전자로 판단되어 일벌 번데기에서 해당 유전자들의 발현 양상을 조사하였다. 두 유전자 모두 유사한 발현 양상을 보이는 것을 확인하였다 (Fig. 2). Alh는 D, V계통이 다른 세 계통과 비교했을 때 유의미하게 높은 수준으로 발현되는 것이 확인되었다 (Fig. 2a). Hr78 역시 D, V계통의 발현이 높았으나 A계통과는 유의성이 확인되지 않았다 (Fig. 2b). 선행연구의 gene ontology (GO)에 따르면 Alh와 Hr78은 DNA 결합 기능을 가지는 것으로 보고되었다 (Navajas et al., 2008). 초파리에서 Alh는 polycomb group-responsive element (PRE)에 결합해 유전자 발현을 조절하는 크로마틴 조절자로 기능하며, PRE는 초파리에서 면역 및 발달 유전자 조절에도 관여한다 (Perrin and Dura, 2004; Kassis and Brown, 2014). Hr78은 초파리에서 ecdysone 신호와 상호작용함으로써 다양한 조직의 유전자 발현을 조절한다. Ecdysone은 곤충의 탈피호르몬으로 기능할 뿐 아니라 선천면역 과정 및 신경세포의 증식과 분화를 조절하는 notch 신호경로를 구성하는 유전자의 발현에 관여한다 (Regan et al., 2013; Tan et al., 2014; Xiong et al., 2016; Marxreiter and Thummel, 2018). Weaver et al. (2021)은 응애 저항성 꿀벌과 감수성 꿀벌 간의 유전자 발현 차이를 보고하였다. 저항성 꿀벌의 경우 감염 스트레스에 노출된 후 항바이러스 반응과 산화 스트레스 및 해독, 신경 및 행동 관련 유전자의 발현이 급격히 유도되었다. Conlon et al. (2019)은 꿀벌 번데기에서 특정 유전자의 발현이 꿀벌응애의 생식을 방해하여 저항성 획득에 관여한다는 것을 보였다. 꿀벌응애는 ecdysteroid를 자체적으로 합성하지 못해 숙주인 꿀벌로부터 의존적으로 획득하여 vitellogenesis를 개시한다. 이때 ecdysone 연관 유전자의 발현 조절은 기생-숙주 간 생리 시계 불일치를 일으켜 꿀벌응애의 생식 실패를 유도한다 (Tewarson, 1982; Cabrera et al., 2015; Conlon et al., 2018; Conlon et al., 2019). 따라서 본 연구에서 보인 해당 유전자들의 발현 증가는 이들이 전사조절 인자로 기능하면서 감염이나 스트레스 상황에서 면역 및 조직 항상성과 관련된 유전자들의 발현을 간접적으로 조절할 가능성을 시사한다. 전사조절 유전자의 발현 증가는 생리적 신호 조절을 통해 기생충 감염을 방어하는 전략일 수 있으며, 계통별 발현 차이를 고려했을 때 D, V계통이 꿀벌응애 감염에 대한 저항성이 우수할 것으로 예상된다.
3. Varroa-sensitive hygiene (VSH) 유전자 분석
실험에 앞서 꿀벌의 머리, 가슴, 배에서 각각 VSH 유전자의 발현을 조사하였다 (Table 3). 그 결과 기존 연구와 동일하게 머리에서 현저히 높은 수준으로 발현되는 것을 확인하여 이후 VSH 유전자는 하인두샘과 겹눈 등을 제거한 내역봉의 뇌조직만을 사용하였다 (Fig. 3). VSH 유전자는 크게 위생행동을 보이는 꿀벌 (hygienic bee; HB)과 위생행동을 하지 않는 꿀벌 (non-hygienic bee; NHB)에서 각각 발현 증가가 보고된 유전자로 나누어 분석하였다. 더하여 위생행동에 따른 발현 차이는 보고된 바 없으나 이에 관여할 가능성이 높은 후각 관련 유전자 2개를 추가로 분석하였다. 일부 유의미한 발현 차이를 보이는 유전자가 확인되었다.
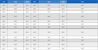
Relative mRNA expression levels in each body parts in honeybees (head, thorax, and abdomen). (a) Arrestin 2, (b) antennal dehydrogenase (Antdh), (c) long-wavelength sensitive opsin 1 (Lop1). Different letters indicate significant differences. One-way ANOVA following Tukey̓s HSD (P<0.05).
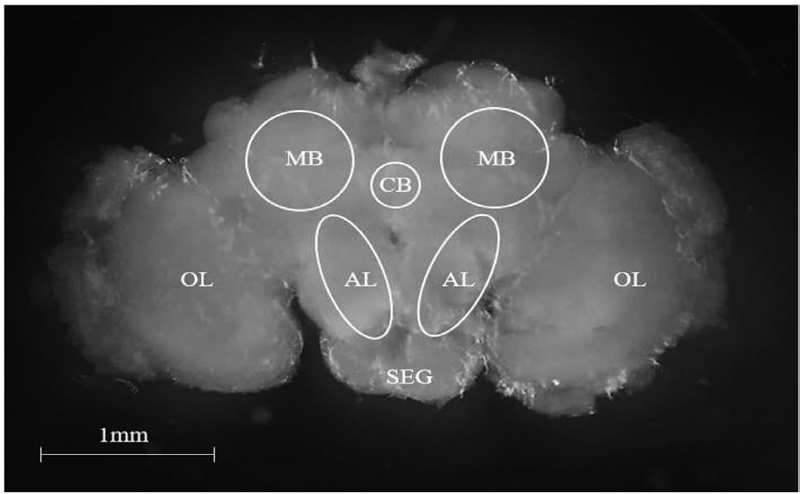
Dissected honeybee brain. Mushroom bodies (MB), central body (CB), antennal lobes (AL), optical lobes (OL), and subesophageal ganglion (SEG) indicated. Scale bar, 1 mm.
HB에서 발현 증가가 보고된 유전자 그룹은 전반적으로 A계통에서 낮게 발현되는 경향을 보이는 가운데 Myosin 20 (Myo20)과 Syntrophin-like 1 (Syn1)은 V계통에서 높은 수준으로 발현하였다. D계통은 Myosin 20의 발현이 가장 낮았으며, F계통은 다른 계통들과 유의미한 차이를 보이지 않았다 (Fig. 4a, b). Myo20과 Syn1은 감염된 유충 또는 번데기 제거 행동과 연관된 QTL인 removal 1 (Rem1) 영역에 존재하는 유전자이다 (Oxley et al., 2010; Boutin et al., 2015). Myo20과 같은 Myosin 유전자군은 일반적으로 근육과 관련된 것으로 여겨지나, Liao et al. (2024)의 연구 결과에 따르면 꿀벌응애 감염 시 몸단정 행동의 빈도와 강도 조절에 관여하며 꿀벌의 신경 및 시각 시스템에 역시 중요한 기능을 가진다 (Calábria et al., 2011; Southey et al., 2016). 초파리에서 Syn1은 신경 형성과 관련된 기능을 가지고 신경전달 및 행동 패턴 형성과의 연관성이 제시되었다 (Turner et al., 2013). 또한 HB와 NHB 사이에 보고된 Syn1의 단일염기 다형성 (Single nucleotide polymorphism; SNP)은 염기서열 변이로 인한 행동 기능 차이가 꿀벌의 위생행동을 결정할 수 있다는 것을 나타낸다 (Teixeira et al., 2021). Cuticular protein 5 (CPR5)는 D계통에서 가장 높게 발현되었으나, A계통을 제외한 나머지 계통과는 유의미한 차이를 확인할 수 없었다 (Fig. 4c). Cuticular protein은 구조단백질로 세포골격 유지 기능을 가지는 것으로 알려져 있지만 곤충의 뇌에서 가지는 기능은 현재 연구가 이루어지지 않았다. Protein kinase A (PKA)는 곤충 뇌의 학습 및 기억에 관여하는 버섯체 (mushroom body)에서 특이적으로 발현되어 cAMP-PKA 경로를 통해 꿀벌의 장기기억을 형성하며, 학습 및 기억 회로에서 중요한 역할을 가진다 (Müller, 1998; Eisenhardt, 2006). 이번 연구에서 cAMP-dependent protein kinase 1 (Pka-C1)은 모든 계통에서 유의미한 발현 차이를 확인하지 못했으나 (Fig. 4d), Teixeira et al. (2021)의 연구에서 보인 HB와 NHB 간 Pka-C1의 SNP 변이는 해당 유전자가 발현 수준에서는 유의미한 차이를 보이지 않더라도 염기서열 구조 변이로 인한 기능적 차이를 유발할 수 있다는 것을 나타낸다.
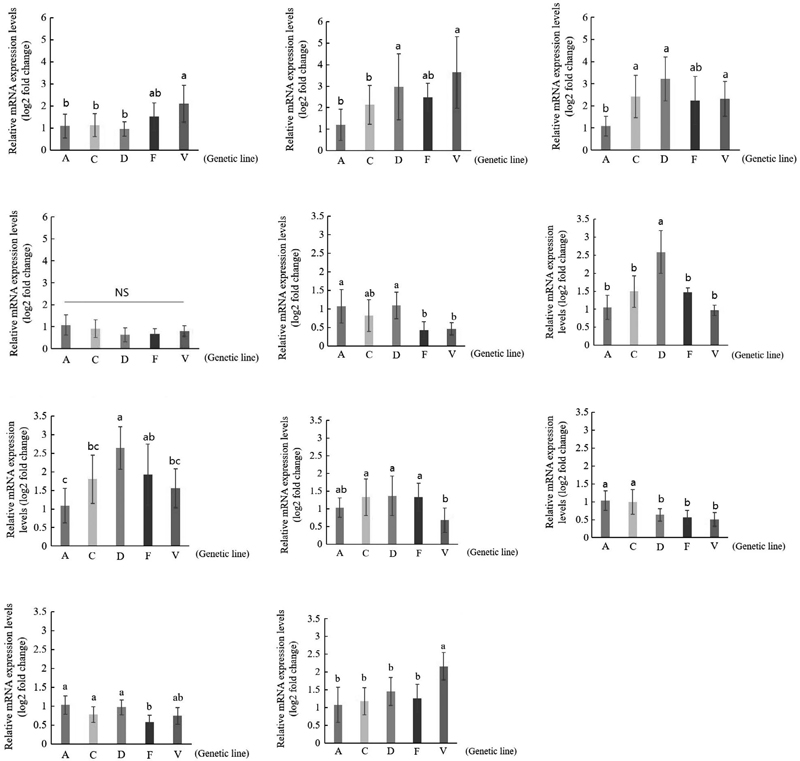
Relative mRNA expression levels of Varroa-sensitive hygiene (VSH) genes between different strains of honeybees. (a) Myosin 20, (b) syntrophin-like 1, (c) cuticular protein 5, (d) cAMP-dependent protein kinase 1, (e) arrestin 2, (f) antennal dehydrogenase, (g) long-wavelength sensitive opsin 1, (h) odorant binding protein 4, (i) down syndrome cell adhesion molecule, (j) octopamine receptor, (k) odorant binding protein 1. Different letters indicate significant differences. Kruskal-Wallis following Dunn’s test (P<0.05).
NHB에서 발현 증가가 보고된 유전자 그룹은 대체로 A, C, D계통에서 발현이 증가하는 경향을 보였다 (Fig. 4e-i). Arrestin 2, odorant binding protein 4 (Obp4), 그리고 down-syndrome cell adhesion molecule (Abscam)은 V계통과 F계통에서 낮게 발현되는 것을 보였으며 F계통의 경우 Obp4의 발현은 A, C, D계통과 유의성이 없었으나 arrestin 2와 Abscam은 V계통과 유사한 발현량을 보였다 (Fig. 4e, h and i). Antennal dehydrogenase (Antdh)와 long-wavelength sensitive opsin 1 (Lop1)은 D계통에서 가장 높게 발현되었다 (Fig. 4f, g). Arrestin 2와 Lop1은 시각 신호에 관여하며, arrestin 2는 후각 뉴런에서도 발현되어 중요한 기능을 가진다 (Dolph et al., 1993; Mondragón et al., 2005; Walker et al., 2008). Le Conte et al. (2011)에서는 시각 신호 유전자들의 하향 조절에 대해 HB가 NHB보다 더 많은 시간을 어두운 봉군 내에서 보내면서 위생행동을 수행하기 때문이라고 추측하였다. Abscam은 A, C계통에서 발현 증가를 보였다 (Fig. 4i). Abscam 또한 초파리에서 후각신호에 관여하고 축삭 유도 기능을 가지는 세포 접착 단백질을 암호화한다 (Hummel et al., 2003; Teixeira et al., 2021). 꿀벌에서는 뇌에서 발현되며 우화 후 시간이 경과함에 따라 발현이 감소한다 (Funada et al., 2007). 이와 같은 발현 특성은 우화 직후 후각 신경망의 안정화와 후각 기반 행동 학습에 관여할 수 있다는 것을 보인다. NHB에서는 주로 후각 및 시신경 등 감각 연관 유전자들의 발현 증가가 확인되었다 (Oxley et al., 2010; Le Conte et al., 2011; Boutin et al., 2015). 번데기의 체액은 후각 자극을 통해 일벌들의 위생행동을 촉진하는 주요 인자로 알려져 있다 (Gramacho and Spivak, 2003). 위생 행동의 빈도와 개시 시점은 후각 자극에 대한 반응 임계값 (task threshold)에 의해서 결정된다. HB와 NHB는 반응 임계값에 뚜렷한 차이를 보인다. HB는 후각 민감도가 높아 비교적 낮은 수준의 자극에도 빠르게 반응하지만 (Masterman et al., 2001; Gramacho and Spivak, 2003; Ivanova and Bienefeld, 2023), 실제 분석에서는 역설적으로 NHB에서 후각 관련 유전자들의 발현 증가가 확인되었다. 이는 HB가 후각 자극에 대해 민감하다는 기존 가설과 일치하지 않으며, Le Conte et al. (2011)의 연구 역시 이 점을 지적하였다. 기존 가설과 모순되지 않는 해석으로 NHB들이 HB와 비교했을 때 자극에 대해 낮은 감도를 가지고, 반응 임계값이 높아 이에 대한 보상작용으로 감각신호 전달 유전자들의 발현량이 증가하는 것으로 추측된다. 후각 신호를 통한 행동 조절은 초파리에서 이미 보고된 바 있으며, HB에서 발현이 증가하는 후각 관련 유전자 역시 존재한다 (Anholt et al., 2001; Dubnau et al., 2003; Navajas et al., 2008).
선행 연구에서 HB와 NHB 사이에 별도의 발현 차이가 보고된 적 없는 Octopamine receptor (OcR)와 Odorant binding protein 1 (Obp1)을 추가로 분석하였다 (Fig. 4j, k). Octopamine은 후각 기억의 형성에 필수적이며 후각 자극을 제시했을 때 위생행동을 개시하는 시점이 빠른 꿀벌의 뇌에서 발현이 증가한다 (Farooqui et al., 2003; Spivak et al., 2003). Obp1은 꿀벌의 행동 또는 후각 학습에 영향을 미치는 Hyg1 QTL 영역에 존재한다 (Oxley et al., 2010). qPCR 결과 OcR은 F계통에서 가장 낮은 발현을 보이며 그 밖의 다른 계통끼리는 유의미한 발현 차이를 확인할 수 없었다 (Fig. 4j). Obp1은 V계통에서 가장 높게 발현되었고 다른 계통간 유의성은 확인되지 않았다 (Fig. 4k).
꿀벌의 응애 저항성과 위생행동은 특정 유전자들로만 결정되는 것이 아닌 해당 형질에 관여하는 수많은 유전자들로 인해 결정되는 양적형질이다. 본 연구에서 보인 후각 신호 관련 유전자들의 일관적이지 않은 발현은 단순히 유전자의 발현량뿐 아니라 SNP와 같은 염기서열의 변이와 같은 요인들이 꿀벌의 위생행동에 영향을 미친다는 것을 시사한다. 기존 연구결과에서 역시 모든 유전자들이 보고된 것과 동일한 발현을 보이지는 않았다 (Teixeira et al., 2021). 대신 일부 유전자들에 존재하는 SNP가 유전자 발현이나 기능에 영향을 미침으로써 꿀벌의 응애 저항성 또는 위생행동을 결정할 수 있다는 것이 밝혀졌다 (Conlon et al., 2019; Teixeira et al., 2021). 본 연구에서 사용된 꿀벌 유전자원 역시 기존 연구에 사용된 꿀벌과 다른 만큼 이들의 유전적 차이로 인해 발현이 달라질 가능성이 있으나, 계통간 분석 결과 꿀벌응애 저항성과 관련된 일부 유전자의 발현 차이를 확인하였다. 계통별 발현 양상의 차이는 VSH 수준과 저항성 차이를 반영할 수 있음을 나타낸다.
본 연구에서 활용된 유전자들이 꿀벌에서 가지는 기능은 현재 명확하지 않으나, 선행 연구 및 초파리에서 보고된 상동 유전자의 기능을 바탕으로 꿀벌응애 저항성에 대한 잠재적 기능을 추측하였다. 꿀벌의 응애 저항성 획득 기작을 이해하기 위해서 해당 유전자들의 기능을 규명할 필요가 있다. 본 연구 결과를 바탕으로 꿀벌응애 저항성 품종 육성 시 최우선 후보군은 V계통, 차순으로 D 또는 F계통을 후보군으로 이용 가능할 것으로 판단된다. 추후 유전자 발현과 실제 위생행동 간의 추가 분석을 통해 후보군 선발의 정밀성을 높이고 효율적인 저항성 품종 개발에 기여 가능할 것으로 기대된다.
적 요
현재 월동폐사로 인한 피해사례가 매년 지속적으로 보고되고 있다. 안정적인 월동을 위해서는 주요 원인 중 하나인 꿀벌응애 방제가 필수적이다. 나아가 근본적인 해결책으로 꿀벌응애 저항성 품종의 육성이 필요하다. 이에 국외 연구 사례를 참조하여 꿀벌 유전자원을 대상으로 꿀벌응애 저항성 연관 유전자의 발현을 분석하였다. TANC2와 baz는 전용유충보다는 번데기에서 크게 발현이 증가하였다. 이는 꿀벌응애 감염 및 가해 시점에 반응해 발현이 상향조절된다는 것을 나타낸다. 추후 꿀벌응애 저항성 기작을 밝히기 위해 해당 유전자들의 기능 규명이 필요하다. 꿀벌응애 저항성과 관련된 유전자들의 꿀벌 계통 (A, C, D, F, V) 간 발현 양상을 분석한 결과 D, V계통에서 Alh, Hr78의 유의미한 발현 증가를 확인하였다. 이는 D, V계통이 꿀벌응애 감염에 대한 저항성이 높을 수 있다는 것을 시사한다. VSH 유전자는 일관성 있는 발현 양상을 보이지 않았으나 마찬가지로 V계통에서 발현에 유의미한 차이를 보이는 유전자를 다수 확인하였다. D, F계통에서 또한 일부 유전자의 유의미한 발현이 확인되었다. 추후 계통간 실제 위생행동과 유전자 발현 간의 상관분석을 통해 후보군 선발에 보다 적합한 기준을 세울 수 있을 것으로 예상된다.
Acknowledgments
본 연구는 농촌진흥청 연구과제 PJ1418007의 연구비로 수행되었으며 2025년 농촌진흥청 국립농업과학원 전문연구원 과정 지원 사업에 의해 이루어졌습니다.
References
-
Anholt, R. R., R. F. Lyman and T. F. Mackay. 2001. Functional genomics of odor-guided behavior in Drosophila melanogaster. Chem. Senses 26(2): 215-221.
[https://doi.org/10.1093/chemse/26.2.215]

-
Bailey, L., A. J. Gibbs and R. D. Woods. 1963. Two viruses from adult honey bees (Apis mellifera Linnaeus). Virology 21(3): 390-395.
[https://doi.org/10.1016/0042-6822(63)90200-9]

-
Berthoud, H. 2010. Virus infections and winter losses of honey bee colonies (Apis mellifera). J. Apic. Res. 49(1): 60-65.
[https://doi.org/10.3896/IBRA.1.49.1.08]

-
Boot, W. J., J. N. M. Calis and J. Beetsma. 1992. Differential periods of Varroa mite invasion into worker and drone cells of honey bees. Exp. Appl. Acarol. 16: 295-301.
[https://doi.org/10.1007/BF01218571]

-
Boutin, S., M. Alburaki, P. L. Maercier, P. Giovenazzo and N. Derome. 2015. Differential gene expression between hygienic and non-hygienic honeybee (Apis mellifera L.) hives. BMC Genomics 16(1): 500.
[https://doi.org/10.1186/s12864-015-1714-y]

-
Büchler, R., M. Kovačić, M. Buchegger, Z. Puškadija, A. Hoppe and E. W. Brascamp. 2020. Evaluation of traits for the selection of Apis mellifera for resistance against Varroa destructor. Insects 11(9): 618.
[https://doi.org/10.3390/insects11090618]

-
Burgett, M., P. Akratanakul and R. A. Morse. 1983. Tropilaelaps Clareae: a parasite of honeybees in South-East Asia. Bee World 64(1): 25-28.
[https://doi.org/10.1080/0005772X.1983.11097904]

-
Cabrera, A. R., P. D. Shirk, J. D. Evans, K. Hung, J. Sims, H. Alborn and P. E. Teal. 2015. Three halloween genes from the Varroa mite, Varroa destructor (Anderson & Truman) and their expression during reproduction. Insect Mol. Biol. 24(3): 277-292.
[https://doi.org/10.1111/imb.12155]

-
Calábria, L. K., P. M. V. Peixoto, A. B. P. Lima, L. G. Peixoto, V. R. A. de Moraes, R. R. Teixeira, C. T. dos Santos, L. O. Silva, M. F. R. da Silva, A. A. D. dos Santos, N. Garcia-Cairasco, A. R. Martins, E. M. Espreafico and F. S. Espindola. 2011. Myosins and DYNLL1/LC8 in the honey bee (Apis mellifera L.) brain. J. Insect Physiol. 57: 1300-1311.
[https://doi.org/10.1016/j.jinsphys.2011.06.005]

-
Chen, Y., J. Evans and M. Feldlaufer. 2006. Horizontal and vertical transmission of viruses in the honey bee, Apis mellifera. J. Invertebr. Pathol. 92: 152-159.
[https://doi.org/10.1016/j.jip.2006.03.010]

-
Chen, Y. P., J. S. Pettis, M. Corona, W. P. Chen, C. J. Li, M. Spivak, P. K. Visscher, G. DeGrandi-Hoffman, H. Boncristiani, Y. Zhao, D. van Engelsdorp, K. Delaplane, L. Solter, F. Drummond, M. Kramer, W. I. Lipkin, G. Palacios, M. C. Hamilton, B. Smith, S. K. Huang, H. Q. Zheng, J. L. Li, X. Zhang, A. F. Zhou, L. Y. Wu, J. Z. Zhou, M. Lee, E. W. Teixeira, Z. G. Li and J. D. Evans. 2014. Israeli acute paralysis virus: epidemiology, pathogenesis and implications for honey bee health. PLoS Pathog. 10: e1004261.
[https://doi.org/10.1371/journal.ppat.1004261]

-
Choi, Y. S., M. L. Lee, H. S. Sim, H. K. Kim, G. H. Byeon, M. Y. Yoon, A. R. Kang, T. T. Van and S. O. Woo. 2014. Morphological analysis and determination of interference competition between two honey bee mites: Varroa destructor and Tropilaelaps clareae (Acari: Varroidae and Laelapidae). J. Apic. 29(4): 327-332.
[https://doi.org/10.17519/apiculture.2014.11.29.4.327]

-
Conlon, B. H., E. Frey, P. Rosenkranz, L. Barbara, R. F. A. Moritz and R. Jarkko. 2018. The role of epistatic interactions underpinning resistance to parasitic Varroa mites in haploid honeybee (Apis mellifera) drones. J. Evol. Biol. 31(6): 801-809.
[https://doi.org/10.1111/jeb.13271]

-
Conlon, B. H., A. Adriana, A. L. Giurgiu, J. Kefuss, D. S. Dezmirean, R. F. A. Moritz and J. Routtu. 2019. A gene for resistance to the Varroa mite (Acari) in honey bee (Apis mellifera) pupae. Mol. Ecol. 28(12): 2958-2966.
[https://doi.org/10.1111/mec.15080]

-
Cox-Foster, D. L., S. Conlan, E. C. Holmes, G. Palacios, J. D. Evans, N. A. Moran, P. L. Quan, T. Briese, M. Horing, D. M. Geiser, V. Martinson, D. van engelsdorp, A. L. Kalkstein, A. Drysdale, J. Hui, J. Zhai, L. Cui, S. K. Hutchison, J. F. Simons, M. Egholm, J. S. Pettis and W. I. Lipkin. 2007. A metagenomic survey of microbes in honey bee colony collapse disorder. Science 318: 283-287.
[https://doi.org/10.1126/science.1146498]

-
Danka, R. G., J. W. Harris and G. E. Dodds. 2016. Selection of VSH-derived “pol-line” honeybees and evaluation of their Varroa-resistance characteristics. Apidologie 47: 483-490.
[https://doi.org/10.1007/s13592-015-0413-7]

-
Delfinado, M. D. E. and W. Baker. 1961. Tropilaelaps, a new species of mite from the Philippines (Laelaptidae [s. lat]: Acarina). Fieldiana Zool. 44: 53-56.
[https://doi.org/10.5962/bhl.title.3227]

-
Desai, S. D. and R. W. Currie. 2016. Effects of wintering environment and parasite-pathogen interactions on honey bee colony loss in north temperate regions. PLoS One 11(7): e0159615.
[https://doi.org/10.1371/journal.pone.0159615]

-
Dolph, P. J., R. Ranganathan, N. J. Colley, R. W. Hardy, M. Socolich and C. S. Zuker. 1993. Arrestin function in inactivation of G-protein-coupled receptor rhodopsin in vivo. Science 260: 1910-1916.
[https://doi.org/10.1126/science.8316831]

-
Dubnau, J., A. S. Chiang, L. Grady, J. Barditch, S. Gossweiler, J. McNeil, P. Smith, F. Buldoc, R. Scott, U. Certa, C. Broger and T. Tully. 2003. The staufen/pumilio pathway is involved in Drosophila long-term memory. Curr. Biol. 13(4): 286-296.
[https://doi.org/10.1016/S0960-9822(03)00064-2]

-
Eisenhardt, D. 2006. Learning and memory formation in the honeybee (Apis mellifera) and its dependency on the cAMP-protein kinase A pathway. Anim. Biol. 56(2): 259-278.
[https://doi.org/10.1163/157075606777304249]

-
Farooqui, T., K. Robinson, H. Vaessin and B. H. Smith. 2003. Modulation of early olfactory processing by an octopaminergic reinforcement pathway in the honeybee. J. Neurosci. 23(12): 5370-5380.
[https://doi.org/10.1523/JNEUROSCI.23-12-05370.2003]

-
Funada, M., H. Hara, H. Sasagawa, Y. Kitagawa and T. Kadowaki. 2007. A honey bee Dscam family member, AbsCAM, is a brain-specific cell adhesion molecule with the neurite outgrowth activity which influences neuronal wiring during development. Eur. J. Neurosci. 25(1): 168-180.
[https://doi.org/10.1111/j.1460-9568.2006.05270.x]

-
Gisder, S., P. Aumeier and E. Genersch. 2009. Deformed wing virus: replication and viral load in mites (Varroa destructor). J. Gen. Virol. 90(2): 463-467.
[https://doi.org/10.1099/vir.0.005579-0]

-
Govan, V., N. Leat, M. Allsopp and S. Davison. 2000. Analysis of the complete genome sequence of acute bee paralysis virus show that it belongs to the novel group of insect-infecting RNA viruses. Virology 277: 457-463.
[https://doi.org/10.1006/viro.2000.0616]

-
Gramacho, K. P. and M. Spivak. 2003. Differences in olfactory sensitivity and behavioral responses among honey bees bred for hygienic behavior. Behav. Ecol. Sociobiol. 54: 472-479.
[https://doi.org/10.1007/s00265-003-0643-y]

-
Grindrod, I. and S. J. Martin. 2023. Varroa resistance in Apis cerana: a review. Apidologie 54: 14.
[https://doi.org/10.1007/s13592-022-00977-8]

-
Guzmán-Novoa, E., L. Eccles, Y. Calvete, J. Mcgowan, P. G. Kelly and A. Correa-Benítez. 2010. Varroa destructor is the main culprit for the death and reduced populations of overwintered honey bee (Apis mellifera) colonies in Ontario, Canada. Apidologie 41: 443-450.
[https://doi.org/10.1051/apido/2009076]

-
Hamiduzzaman, M. M., B. Emsen, G. J. Hunt, S. Subramanyam, C. E. Williams, J. M. Tsuruda and E. Guzman-Novoa. 2017. Differential gene expression associated with honeybee grooming behavior in response to Varroa mites. Behav. Genet. 47(3): 335-344.
[https://doi.org/10.1007/s10519-017-9834-6]

-
Highfield, A. C., A. El Nagar, L. C. Mackinder, L. M. Noël, M. J. Hall, S. J. Martin and D. C. Schroeder. 2009. Deformed wing virus implicated in overwintering honeybee colony losses. Appl. Environ. Microbiol. 75(22): 7212-7220.
[https://doi.org/10.1128/AEM.02227-09]

-
Hummel, T., M. L. Vasconcelos, J. C. Clemens, Y. Fishilevich, L. B. Vosshall and S. L. Zipursky. 2003. Axonal targeting of olfactory receptor neurons in Drosophila is controlled by Dscam. Neuron 37(2): 221-231.
[https://doi.org/10.1016/S0896-6273(02)01183-2]

-
Insolia, L., R. Molinari, S. R. Rogaers, G. R. Williams, F. Chiaromaonte and M. Calovi. 2022. Honey bee colony loss linked to parasites, pesticides and extreme weather across the United States. Sci. Rep. 12: 20787.
[https://doi.org/10.1038/s41598-022-24946-4]

-
Ivanova, I. and K. Bienefield. 2023. Apis mellifera worker bees selected for Varroa-sensitive hygiene show higher specific sensitivity and perception speed towards low concentrations of chemical cues emitted by the brood. J. Insect Behav. 36: 96-112.
[https://doi.org/10.1007/s10905-023-09824-9]

- Jung, C. 2008. Economic value of honeybee pollination on major fruit and vegetable crop in Korea. J. Apic. 23(2): 147-152.
-
Kang, Y., S. H. Kwon and C. Jung. 2024. Correlation analysis between honeybee pest occurrences and winter failure based on the questionnaire from beekeepers in Korea. J. Apic. 39(3): 185-193.
[https://doi.org/10.17519/apiculture.2024.09.39.3.185]

-
Kassis, J. A. and J. L. Brown. 2014. Polycomb group response elements in Drosophila and vertebrates. Adv. Genet. 81: 83-118.
[https://doi.org/10.1016/B978-0-12-407677-8.00003-8]

-
Kim, H. K. 2022. The effect of honey bee mites on the winter colony losses. J. Apic. 37(3): 291-299.
[https://doi.org/10.17519/apiculture.2022.09.37.3.291]

-
Kim, M., B. H. Kim, S. Kim, T. A. Tai, J. M. Kim, S. Kim and B. S. Yoon. 2019. Development of ultra-rapid nested PCR method for detection of specific gene of Tracheal mite (Acarapis woodi) J. Apic. 34(1): 15-26.
[https://doi.org/10.17519/apiculture.2019.04.34.1.15]

-
Kim, Y. H. and S. H. Lee. 2022. Current status of fluvalinate resistance in Varroa destructor in Korea and suggestion for possible solution. J. Apic. 37(3): 301-313.
[https://doi.org/10.17519/apiculture.2022.09.37.3.301]

-
Lanzi, G., J. R. Miranda, M. B. Boniotti, C. E. Cameron, A. Lavazza, L. Capucci, S. M. Camazine and C. Rossi. 2006. Molecular and biological characterization of deformed wing virus of honeybees (Apis mellifera L.). J. Virol. 80(10): 4998-5009.
[https://doi.org/10.1128/JVI.80.10.4998-5009.2006]

-
Lapidge, K. L., B. P. Oldroyd and M. Spivak. 2002. Seven suggestive quantitative trait loci influence hygienic behavior of honey bees. Naturwiss 89: 565-568.
[https://doi.org/10.1007/s00114-002-0371-6]

-
Le Conte, Y., C. Alaux, J. F. Martin, J. R. Harbo, J. W. Harris, C. Dantec, D. Séverac, S. Cros-Arteil and M. Navajas. 2011. Social immunity in honeybees (Apis mellifera): transcriptome analysis of varroa-hygienic behavior. Insect Mol. Biol. 20(3): 399-408.
[https://doi.org/10.1111/j.1365-2583.2011.01074.x]

-
Lee, J., K. H. Moon, S. Cho, Y. Lim, S. Kim, S. B. Kim, S. M. Han, Y. H. Kim and S. H. Lee. 2023. Establishment and application of bioassay-and molecular marker-based methods for monitoring fluvalinate resistance of Varroa mites. Pestic. Biochem. Physiol. 197: 105655.
[https://doi.org/10.1016/j.pestbp.2023.105655]

-
Lee, J., J. H. Lee, Y. Lim, S. Cho, K. H. Moon, S. Kim, Y. H. Kim and S. H. Lee. 2025. Rapid spread of amitraz resistance linked to a unique T115N mutation in the octopamine receptor of Varroa mites in Korea. Pestic. Biochem. Physiol. 210: 106387.
[https://doi.org/10.1016/j.pestbp.2025.106387]

-
Liao, J., K. Wan, Y. Lü, W. Ouyang, J. Huang, L. Zheng, L. Miao, S. Su and Z. Li. 2024. Comparison of brain gene expression profiles associated with auto-grooming behavior between Apis cerana and Apis mellifera infested by Varroa destructor. Genes 15: 763.
[https://doi.org/10.3390/genes15060763]

-
Martin, S. J., A. C. Highfield, L. Brettell, E. M. Villalobos, G. E. Budge, M. Powell, S. Nikaido and D. C. Schroeder. 2012. Global honey bee viral landscape altered by a parasitic mite. Science 336 (6086): 1304-1306.
[https://doi.org/10.1126/science.1220941]

-
Marxreiter, S. and C. S. Thummel. 2018. Adult functions for the Drosophila DHR78 nuclear receptor. Dev. Dyn. 247(2): 315-322.
[https://doi.org/10.1002/dvdy.24608]

-
Masterman, R., R. Ross, K. Mesce and M. Spivak. 2001. Olfactory and behavioral response threshold to odors of diseased brood differ between hygienic and non-hygienic honey bees (Apis mellifera L.). J. Comp. Physiol. A. 187(6): 441-452.
[https://doi.org/10.1007/s003590100216]

-
Minaud, E., F. Rebaudo, G. Mainardi, P. Vardakas, F. Jatjina, I. Steffan-Dewenter and F. Requier. 2024. Temperature in overwintering honey bee colonies reveals brood status and predicts colony mortality. Ecol. Indic. 169: 112961.
[https://doi.org/10.1016/j.ecolind.2024.112961]

-
Mondragón, L., M. Spivak and R. Vandame. 2005. A multifactorial study of the resistance of Africanized hybrid honey bees Apis mellifera to the mite Varroa destructor over one year in Mexico. Apidologie 36: 345-358.
[https://doi.org/10.1051/apido:2005022]

-
Müller, U. 1998. Neuronal cAMP-dependent protein kinase type II is concentrated in mushroom bodies of Drosophila melanogaster and the honeybee Apis mellifera. J. Neurobiol. 33(1): 33-44.
[https://doi.org/10.1002/(SICI)1097-4695(199707)33:1<33::AID-NEU4>3.0.CO;2-E]

-
Navajas, M., A. Migeon, C. Alaux, M. L. Martin-Magniette, G. E. Robinson, J. D. Evans, S. Cros-Arteil, D. Crauser and Y. Le Conte. 2008. Differential gene expression of the honey bee Apis mellifera associated with Varroa destructor infection. BMC Genomics 9: 301.
[https://doi.org/10.1186/1471-2164-9-301]

-
Oh, H., T. Begna and C. Jung. 2024. Evaluating the efficacy of registered acaricides on Varroa destructor and Tropilaelaps mercedesae, in Apis mellifera colonies. J. Apic. 39(1): 21-30.
[https://doi.org/10.17519/apiculture.2024.04.39.1.21]

-
O’Shea-Wheller, T. A., F. D. Rinkevich, R. G. Danka, M. Simone-Finstrom, P. G. Tokarz and K. B. Healy. 2022. A derived honey bee stock confers resistance to Varroa destructor and associated viral transmission. Sci. Rep. 12: 4852.
[https://doi.org/10.1038/s41598-022-08643-w]

-
Oxley, P. R., M. Spivak and B. P. Oldroyd. 2010. Six quantitative trait loci influence task thresholds for hygienic behaviour in honeybees (Apis mellifera). Mol. Ecol. 19(7): 1452-1461.
[https://doi.org/10.1111/j.1365-294X.2010.04569.x]

-
Perrin, L. and J. M. Dura. 2004. Molecular genetics of the Alhambra (Drosophila AF10) complex locus of Drosophila. Mol. Genet. Genomics 272: 156-161.
[https://doi.org/10.1007/s00438-004-1042-4]

-
Regan, J. C., A. S. Brandão, A. B. Leitão, Â.R. Mantas Dias, É. Sucena, A. Jacinto and A. Zeidman-Rémy. 2013. Steroid hormone signaling is essential to regulate innate immune cells and fight bacterial infection in Drosophila. PLoS Pathog. 9(10): e1003720.
[https://doi.org/10.1371/journal.ppat.1003720]

-
Requier, F., L. Garnery, P. L. Kohl, H. K. Njove, C. W. W. Prik, R. M. Crewe and I. Steffan-Dewenter. 2019. The conservation of native honey bees is crucial. Trends. Ecol. Evol. 34(9): 789-798.
[https://doi.org/10.1016/j.tree.2019.04.008]

-
Rinderer, T. E., L. I. de Guzman, G. T. Delatte, J. A. Stelzer, V. A. Lancaster, V. Kuznetsov, L. Beaman, R. Watts and J. W. Harris. 2001. Resistance to the parasitic mite Varroa destructor in honey bees from far-eastern Russia. Apidologie 32(4): 381-394.
[https://doi.org/10.1051/apido:2001138]

-
Roth, M. A., J. M. Wilson, K. R. Tignor and A. D. Gross. 2020. Biology and management of Varroa destructor (Mesostigmata: Varroidae) in Apis mellifera (Hymenoptera: Apidae) colonies. J. Integr. Pest Manag. 11(1): 1-8.
[https://doi.org/10.1093/jipm/pmz036]

-
Rothenbuhler, W. C. 1964. Behavior genetics of nest cleaning in honey bees. IV. responses of F1 and backcross generations to disease-killed blood. Am. Zool. 4: 111-123.
[https://doi.org/10.1093/icb/4.2.111]

- Ruttner, F. 2013. Biogeography and taxonomy of honeybees. Springer Science & Business Media, Berlin, Germany. pp. 284.
-
Ryabov, E. V., G. R. Wood, J. M. Fannon, J. D. Moore, J. C. Bull, D. Chandler, A. Mead, N. Burroughs and D. J. Evans. 2014. A virulent strain of deformed wing virus (DWV) of honeybees (Apis mellifera) prevails after Varroa destructor-mediated, or in vitro, transmission. PLoS Pathog. 10(6): e1004230.
[https://doi.org/10.1371/journal.ppat.1004230]

- Shimanuki, H., N. W. Calderone and D. A. Knox. 1994. Parasitic mite syndrome: the symptoms. Am. Bee J. 134: 827-828.
-
Southey, B. R., P. Zhu, M. K. Carr-Markell, Z. S. Liang, A. Zayed, R. Li, G. E. Robinson and S. L. Rodriguez-Zas. 2016. Characterization of genomic variants associated with scout and recruit behavioral castes in honey bees using whole-genome sequencing. PLoS One 11(1): e0146430.
[https://doi.org/10.1371/journal.pone.0146430]

-
Spivak, M., R. Masterman, R. Ross and K. A. Mesce. 2003. Hygienic behavior in the honey bee (Apis mellifera L.) and the modulatory role of octopamine. J. Neurobiol. 55: 341-345.
[https://doi.org/10.1002/neu.10219]

-
Tan, K. L., I. Vlisidou and W. Wood. 2014. Ecdysone mediated the development of immunity in the Drosophila embryo. Curr. Biol. 24(10): 1145-1152.
[https://doi.org/10.1016/j.cub.2014.03.062]

-
Teixeira, É. W., R. M. de Paiva Daibert, L. A. Glatzl Júnior, M. V. da Silva, M. L. Alves, J. D. Evans and A. L. Toth. 2021. Transcriptomic analysis suggests candidate genes for hygienic behavior in African-derived Apis mellifera honeybees. Apidologie 52(2): 447-462.
[https://doi.org/10.1007/s13592-020-00834-6]

-
Tewarson, N. C. 1982. Immunocytochemical localization of host (Apis mellifera) proteins in growing oocytes of a hemophagous mite (Varroa jacobsoni) by the unlabeled antibody-Enzyme (PAP) method. Invertebr. Reprod. Dev. 5(6): 345-348.
[https://doi.org/10.1080/01651269.1982.10553488]

-
Traynor, K. S., F. Mondet, J. R. de Miranda, M. Techer, V. Kowallik, M. A. Y. Oddie, P. Chantawannakul and A. McAfee. 2020. Varroa destructor: A complex parasite, crippling honey bees worldwide. Trends. Parasitol. 36(7): 592-606.
[https://doi.org/10.1016/j.pt.2020.04.004]

-
Truong, A. T., M. S. Yoo, B. R. Yun, J. E. Kang, J. Noh, T. J. Hwang, S. K. Seo, S. S. Yoon and Y. S. Cho. 2022. Prevalence and pathogen detection of Varroa and Tropilaelaps mites in Apis mellifera (Hymenoptera, Apidae) apiaries in South Korea. J. Apic. Res. 62(4): 804-812.
[https://doi.org/10.1080/00218839.2021.2013425]

-
Turner, T. L., P. M. Miller and V. A. Cochrane. 2013. Combining genome-wide methods to investigate the genetic complexity of courtship song variation in Drosophila melanogaster. Mol. Biol. Evol. 30(9): 2113-2120.
[https://doi.org/10.1093/molbev/mst111]

-
van Alphen, J. J. M. and B. J. Fernhout. 2020. Natural selection, selective breeding, and the evolution of resistance of honeybees (Apis mellifera) against Varroa. Zoological Lett. 6: 6.
[https://doi.org/10.1186/s40851-020-00158-4]

-
Walker, W. B., E. M. Smith, T. Jan and L. J. Zwiebel. 2008. A functional role for Anopheles gambiae Arrestin1 in olfactory signal transduction. J. Insect Physiol. 54: 680-690.
[https://doi.org/10.1016/j.jinsphys.2008.01.007]

-
Weaver, D. B., B. L. Cantarel, C. G. Elsik, D. L. Boncristiani and J. D. Evans. 2021. Multi-tiered analyses of honey bees that resist or succumb to parasitic mites and viruses. BMC Genomics 22: 720.
[https://doi.org/10.1186/s12864-021-08032-z]

-
Wu, J., N. B. Tannan, L. T. Vuong, Y. Koca, G. M. Collu and M. Mlodzik. 2024. Par3/bazooka binds NICD and promotes notch signaling during Drosophila development. Dev. Biol. 514: 37-49.
[https://doi.org/10.1016/j.ydbio.2024.06.009]

-
Xiong, X. P., K. Kurthkoti, K. Y. Chang, J. L. Li, X. Ren, J. Q. Ni, T. M. Rana and R. Zhou. 2016. miR-34 modulates innate immunity and ecdysone signaling in Drosophila. PLos Pathog. 12(11): e1006034.
[https://doi.org/10.1371/journal.ppat.1006034]

-
Yoon, H. J., K. Y. Lee, Y. B. Lee, M. Y. Lee, K. Sankar and J. D. Park. 2021. Current status of insect pollinators use for horticultural crops in Korea. J. Apic. 36(3): 111-123.
[https://doi.org/10.17519/apiculture.2021.09.36.3.111]

-
Yoshida, H., T. J. Fuwa, M. Arima, H. Hamamoto, N. Sasaki, T. Ichimiya, K. Osawa, R. Ueda and S. Nishihara. 2008. Identification of the Drosophila core 1 β1,3-galactosyltransferase gene that synthesizes T antigen in the embryonic central nervous system and hemocytes. Glycobiology 18(12): 1094-1104.
[https://doi.org/10.1093/glycob/cwn094]

-
Zhang, L. and K. G. Ten Hagen. 2019. O-Linked glycosylation in Drosophila melanogaster. Curr. Opin. Struct. Biol. 56: 139-145.
[https://doi.org/10.1016/j.sbi.2019.01.014]