아까시꿀의 미생물 다양성, 기능 연구와 원산지 식별을 위한 환경 DNA 메타바코딩 접근법
Abstract
This study analyzed fifteen domestic and four imported Robinia honey samples using V3-V4 16S rRNA gene metabarcoding, identifying a total of 1,147 bacterial taxa. The 39 most prevalent taxa were grouped into five functional categories based on their physiological and ecological characteristics: (1) honeybee-associated symbionts, such as Apilactobacillus spp. and Gilliamella apicola, which aid in digestion and immune function; (2) pathogenic bacteria, including Melissococcus plutonius and Paenibacillus larvae, responsible for foulbrood diseases; (3) beneficial and probiotic strains like Bacillus atrophaeus, Latilactobacillus sakei, and Clostridium butyricum with fermentative and antimicrobial properties; (4) skin and human commensals, such as Cutibacterium acnes and Staphylococcus capitis, suggestive of potential operator or cross-contamination; and (5) environmental and plant-associated microorganisms, including Pantoea, Acinetobacter, Pseudomonas, and Erwinia, originating from soil, vegetation, and air. These microbial community profiles show potential as biomarkers for verifying honey origin, as well as providing simultaneous insights into apiary health and disease risks.
Keywords:
Robinia honey, Microbial Community, Provenance verification서 론
꿀은 높은 당 함량에도 불구하고 장기간 안정적으로 보존되는 독특한 특성을 지니며, 이러한 특성에는 꿀 속에 존재하는 다양한 미생물군의 역할이 크다. 꿀 내 미생물은 박테리아와 진균류로 구성되며, 그 기원은 밀원식물의 꽃 표면 및 꿀샘에 서식하는 미생물이 꿀벌의 매개를 통해 유입되거나, 꿀벌 자체의 장내 미생물이 꿀에 포함되는 경로, 벌집 주변 환경 미생물의 혼입, 그리고 꿀 채취 및 보관 과정에서 외부 환경 미생물이 꿀에 혼입되는 과정 등으로 다양하다 (Snowdon and Cliver, 1996; Olaitan et al., 2007; Xiong et al., 2023; Luca et al., 2024). 이에 따라 꿀 내 미생물 군집의 구성과 다양성은 밀원식물의 종류와 꿀벌의 건강상태에 따라 달라질 수 있다.
특히, 꿀 내 일부 유용 미생물 종들은 발효 대사 및 유기산 생성에 관여하여 꿀의 pH를 낮추고 화학적 안정성을 향상시켜 품질과 저장성을 증진시키는 데 기여한다 (Avina, 2024). 또한, 꿀 속 미생물군은 병원성 미생물의 증식을 억제하는 항균 환경을 조성하며, 곰팡이 및 박테리아 오염 방지와 함께 꿀벌 건강 및 군집 생태계 유지에 중요한 상호작용을 나타낸다 (Lanh et al., 2024).
최근 DNA 기반 분석기술, 그중에서도 메타바코딩은 식품의 품질관리, 원산지 인증, 병원체 검출 등에 폭넓게 활용되고 있다 (Soares et al., 2023). 꿀을 포함한 다양한 산물에서 메타바코딩을 통한 유전자 분석은 해당 산물의 환경적 배경과 특성을 정확히 반영할 수 있음이 여러 연구를 통해 입증되어 왔다 (Bruni et al., 2015; Laha et al., 2017; Saravanan et al., 2019; Milla et al., 2023; Namin et al., 2022; Letsiou et al., 2024). 본 연구에서는 16S rRNA 유전자를 마커로 활용한 메타바코딩 분석을 통해 꿀 내 미생물 군집이 지리적 원산지 판별에 유용한 생물학적 지표로 활용될 수 있는지 평가하고자 한다.
재료 및 방법
1. 시료
본 연구에서는 사용한 아까시꿀은 Robinia pseudoacacia를 밀원으로 생산한 꿀로 2024년에 채집된 국내산 15종 (강원 1지역, 경기 지역, 충청 지역, 전라 지역, 경상 지역)과 수입산 아까시꿀 3종 (중국산 3개, 베트남 1개)을 대상으로 DNA 메타바코딩 분석을 수행하였다.
2. 꿀 DNA 추출 방법
꿀에서 총 DNA를 추출하기 위하여 꿀에 잔류할 수 있는 DNA (cell-free)와 화분 DNA 모두를 얻기위해 꿀 10 g에 5배 부피의 GI buffer를 첨가한 후 균질하게 혼합 후 13,000 rpm에서 30분간 원심 분리하여 얻은 상층액은 affinity column에 통과시켜 회수하였다. 원심 분리하여 얻은 화분 침전물은 DNeasy Plant Mini Kit (QIAGEN, Hilden, Germany)를 이용하여 제조사 매뉴얼에 따라 DNA를 추출하였다. 이들로부터 얻은 DNA 모두를 합쳐 최종 분석에 사용하였다 (Kim et al., 2024).
3. 라이브러리 준비 및 염기서열 분석
염기서열 분석을 하기 위하여 Illumina 16S 메타유전체 시퀸싱 라이브러리 제작방법에 따라 준비하였다. 사용한 5 ng 혹은 10 ng 꿀 시료 DNA는 5× 반응 버퍼, 1 mM dNTP혼합물, 16S Forward, reverse 프라이머, 500 nM Herculase II fusion DNA 중합효소 (Agilent Technologies, Santa Clara, CA, USA)와 함께 PCR 증폭되었다. 1차 PCR 반응 조건은 열 활성화 단계로 95°C에서 30초, 55°C에서 30초, 72°C에서 30초로 25사이클, 그리고 72°C에서 5분간 반응시켰다. 이 반응은 16S V3-V4 범용 프라이머로 Illumina 어댑터 오버행 시퀸스가 포함되어 있는 것을 사용하였다. 그 염기서열은 다음과 같다 (Forward 5ʹ- TCGTCGGCAGCGTCAGATGTGTATAAGAGACAGCCTACGGGNGGCWGCAG-3ʹ, Reverse 5ʹ- GTCTCGTGGGCTCGGAGATGTGTATAAGAGACAGGACTACHVGGGTATCTAATCC-3ʹ). 해당 프라이머는 미생물 군집 분석에 널리 활용되는 표준 프라이머이며 미생물 다양성 평가에 적합하다. 1차 PCR산물은 AMPure 비드 (Agencourt Biosciences, Beverly, MA, USA)로 정제한 후 1차 PCR산물 10 μL를 NexteraXT 인덱스 프라이머를 사용하여 PCR를 수행하였다. 2차 PCR 조건은 98°C에서 1분, 98°C 15초, 55°C에서 15초, 72°C에서 30초 반응을 10회전 한 후 72°C에서 3분간 반응하였다. PCR 산물은 AMPure 비드로 정제하였고 최종 정제된 산물은 KAPAlibrary quantification kit (for Illumina sequencing platforms)를 사용하여 정량하였으며 Tapestation D1000 Screentape (Agilent Technologies, Waldbronn, Germany)를 사용하여 성상분석 후 Illumina MiSeq 플랫폼 (Illumina, San Diego, USA)을 사용하여 시퀀싱을 진행하였다.
4. 데이터 분석
염기서열 대상은 DADA2, Uchime, Filtering하여 불필요한 서열들을 제거하여 얻은 ASV를 NC.I Refseq 16S (Ver. 2024-05-21)데이터베이스와 BLAST 분석하였다. 각 시료에 존재하는 염기서열의 다양성을 나타내는 알파다양성은 Observed ASV, Shannon, Simpson에 기초하여 평가하였고 베타다양성은 weighted Unifrac 거리를 이용하여 분석하여 시각화를 통해 확인하였다.
결 과
1. 아까시꿀에서 미생물종 동정을 위한 DNA barcording
아까시꿀 내 미생물 종 동정을 위한 DNA 바코딩 분석에서는 총 19개 아까시꿀 샘플에서 관찰된 ASV (Amplicon Sequence Variant) 수가 457에서 5,409 사이로 다양하게 나타났다. 종 다양성과 균등도를 나타내는 Shannon 지수는 6.51에서 11.83, Simpson 지수는 0.983에서 0.999 범위 내에 분포하여 높은 다양성을 확인할 수 있었다 (Table 1). 특히 국내산 아까시꿀은 전반적으로 수입산 아까시꿀에 비해 더 높은 종 다양성과 균등도를 보이는 경향이 관찰되었다.
2. 아까시꿀에서 미생물 DNA의 분류종 조성
아까시꿀에서 추출된 미생물 DNA의 분류학적 조성 분석 결과, 총 1,147개의 박테리아 taxon 중 39개 종이 8개 강 (class), 17개 목 (order), 23개 과 (family), 28개 속 (genus)으로 재분류되었다 (Table 2). weighted UniFrac 거리를 기반으로 한 베타다양성 분석에서 국내산과 수입산 아까시꿀의 미생물 군집 구조가 구분되어, 미생물군집이 지리적 특성을 반영함을 보였다 (Fig. 1). 특히 Apilactobacillus 속 2종과 Bombella과, 그리고 Gilliamella 속 각 1종들은 국내산 아까시꿀에서만 현저히 높은 상대적 풍부도를 나타냈으며, 이들 미생물은 꿀벌 장내 공생체로서 꿀벌의 건강과 면역 기능 강화에 기여하는 유익 균주로 알려져 있다. Z-score heatmap 분석 (Fig. 2)은 국내산과 수입산 아까시꿀 시료 간 미생물 군집 내 상대적 풍부도의 차이를 명확히 보여주어, 국내 산지별 미생물 다양성과 군집 구성을 효과적으로 반영함을 확인하였다.
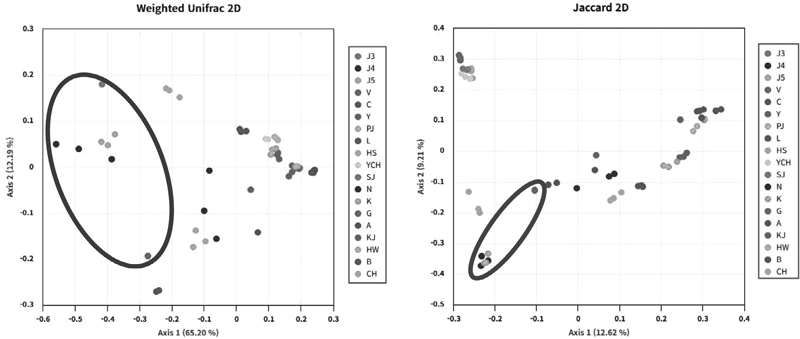
Beta diversity analysis of microbial communities in Robinia honey samples. Beta diversity was evaluated using weighted UniFrac and Jaccard distance metrics to compare the microbial community compositions between domestic and imported Robinia honey samples. Each point represents one of three technical replicates per sample, with colors indicating geographic origin. Circles denote imported honey samples.
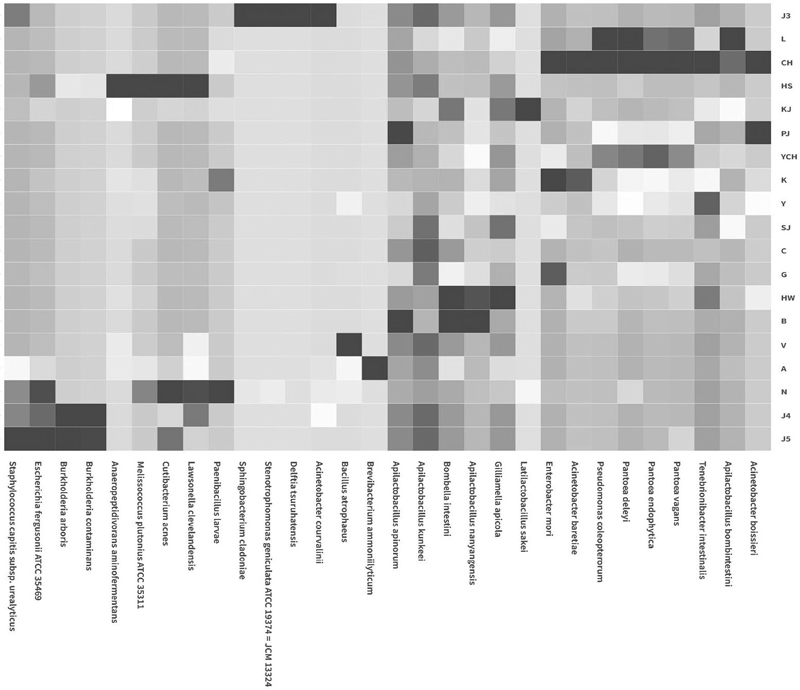
Z-score heatmap of top 30 bacterial species in Robinia honey. The heatmap depicts the standardized relative abundance (Z-score) of the top 30 bacterial taxa across domestic and imported Robinia honey samples. Color gradients indicate variations in microbial abundance, illustrating differences in community composition and diversity between samples of different geographic origins.
고 찰
최근 여러 연구들 (Silva et al., 2017; Vazquez-Quiñones et al., 2018; Santorelli et al., 2023)과 본 연구를 통해 확인된 바와 같이, 꿀에 존재하는 미생물 군집은 꿀벌 장내 공생미생물, 병원체, 프로바이오틱 균주, 인체 피부 공생균 및 환경 기원 미생물 등 다섯 주요 그룹으로 구성된다 (Table 2). 본 연구 대상인 국내산과 수입산 아까시꿀에서 Apilactobacillus 속 2종, Bombella과, Gilliamella 속 미생물은 국내산 시료에서 상대적 풍부도가 높았으며, 이들은 꿀벌의 소화와 면역 기능에 기여하는 장내 공생미생물로 알려져 있다(Lanh et al., 2024; Luca et al., 2024). 이와 더불어, 꿀 내 미생물 조성은 숙성도, 수분 함량, 벌의 이동 경로, 그리고 밀원식물 특성에 따라 다양하게 변동하며 (Wen et al., 2017; Rosli et al., 2020; Santorelli et al., 2023), 가공 및 유통 과정에서 인체 피부 공생균의 혼입 가능성도 존재하기 (Scott et al., 2002)에 원산지 판별 연구에서는 주의가 필요하다.
그럼에도 불구하고, ITS1 마커를 이용한 진균 마이크로바이옴 분석 연구는 꿀의 원산지 판별을 효과적으로 수행할 수 있음을 보여주었고 (Ullah et al., 2024), 환경 및 식물 기원 미생물이 원산지 판별의 주요 지표임이 입증되었다 (Wirta et al., 2021). 스페인에서의 머신러닝 기반 미생물 군집 분석 (Sabater et al., 2024)과 메타바코딩에 물리·화학적 요소를 결합한 분석 (Xiong et al., 2023) 또한 미생물 군집을 활용한 원산지 판별 가능성을 크게 높이고 있다.
본 연구 결과는 산지별 미생물 군집의 상대적 풍부도 차이가 꿀의 지리적 원산지 구별에 유용한 생물학적 지표임을 다시 한 번 시사한다. 향후에는 시료 수 확대, 계절 및 환경 변동성에 따른 미생물 군집 변화 연구가 필요하며, 김치 원산지 판별 (An et al., 2014; Lee et al., 2020) 및 식품원료의 특정 미생물 유전자 기반 원산지 구별 연구 (Winitzingerode et al., 1997; Lee et al., 2015)를 참고하여 꿀 미생물 군집의 정확한 산지 분류를 위한 특이적 분자 마커 개발이 필수적이다. 마지막으로 머신러닝 기반 예측 모델과 표준화되고 체계적인 데이터베이스 구축을 통해 꿀 원산지 판별 체계 개발이 향후 중요한 연구 과제로 제안된다.
Acknowledgments
본 연구는 2025년도 농촌진흥청 국립농업과학원 전문 연구원 과정 지원사업에 의해 이루어진 것이며 국립농업 과학원 농업과학기반기술연구 (과재번호: PJ01745703)에 의하여 수행되었습니다.
References
-
An, D., H. R. Kim, D. W. Jeong, J. M. Caldwell and J. H. Lee 2014. Bacterial Community Monitoring of Commercial Kimchi Produced in Korea and China with Evidence of Bacilli Spore Formation during Fermentation. Korean J. Microbiol. Biotechnol. 42(2): 121-130.
[https://doi.org/10.4014/kjmb.1405.05001]

- Avina, S. 2024. The Microbiology of Honey: A Sweet Symphony of Life. Published: Dec. 20, 2024 American Society for Microbiology.
-
Bruni, I., A. Galiberti, L. Caridi, D. Scaccabarozzi, F. De Mattia, M. Casiraghi and M. Labra. 2015. A DNA barcoding approach to identify plant species in multiflower honey. Food Chem. 170: 308-315.
[https://doi.org/10.1016/j.foodchem.2014.08.060]

-
Hroncova, Z., J. Havlik, J. Killer, I. Doskocil, J. Tyl, M. Kamler, D. Titera, J. Hakl, J. Mrazek, V. Bunesova and V. Rada. 2015. Variation in Honey Bee Gut Microbial Diversity Affected by Ontogenetic Stage, Age and Geographic Location.
[https://doi.org/10.1371/journal.pone.0118707]

-
Kim, S. M., S. O. Woo, H. M. Choi and H. Y. Kim. 2024. DNA metabarcoding-based analysis of plant in Korea Robinia honey. J. Apic. 40(1): 75-81.
[https://doi.org/10.17519/apiculture.2025.04.40.1.75]

-
Laha, R. C., S. De Mandal, L. Ralte, L. Ralte, N. S. Kumar, G. Gurusubramanian, R. Satishkumar, R. Mugasimangalam and N. A. Kuravadi. 2017. Meta-barcoding in combination with palynological inference is a potent diagnostic marker for honey floral composition. AMB Expr. 7: 132.
[https://doi.org/10.1186/s13568-017-0429-7]

-
Lanh, P. T., B. T. T. Duong, H. T. Thu, N. T. Hoa and D. V. Quyen. 2024. Comprehensive analysis of the microbiome in Apis cerana honey highlights honey as a potential source for the isolation of beneficial bacterial strains. PeerJ. Mar 27;12:e17157.
[https://doi.org/10.7717/peerj.17157]

-
Lanubile, A., L. Stagnati, A. Marocco and M. Busconi. 2024. DNA-based techniques to check quality and authenticity of food, feed and medicinal products of plant origin: A review. Trends Food Sci. Technol. 149: 104568.
[https://doi.org/10.1016/j.tifs.2024.104568]

-
Letsiou, S., P. Madesis, E. Vasdekis, C. Montemurro, M. E. Grigoriou, G. Skavdis, V. Moussis, A. E. Koutelidakis and A. G. Tzakos. 2024. DNA barcoing as a plant identification method. Appl. Sci. 14: 1415.
[https://doi.org/10.3390/app14041415]

-
Lee, H. J., G. R. Kim, K. Park, J. Kim and J. H. Kwon. 2015. Effect of electron beam irradiation on microbiological and physicochemical properties of dried red pepper powders of different origin. Korean J. Food Sci. Technol. 47(1): 13-19.
[https://doi.org/10.9721/KJFST.2015.47.1.13]

-
Lee, H. W., S. R. Yoon, J. S. Yang, H. M. Lee, S. J. Kim, J. Y. Lee, I. M. Hwang, S. Y. You and J. H. Ha. 2021. Proteomic evaluation of kimchi, a traditional Korean fermented vegetable, and comparison of kimchi manufactured in China and Korea. J Food Sci Technol. 58(1): 389-396.
[https://doi.org/10.1007/s13197-020-04777-9]

-
Lee, S. K. and H. Lee. 2016. Antimicrobial activity of solvent fractions and bacterial isolates of Korean domestic honey from different floral sources. Food Sci. Biotechnol. 25(5): 1507-1512.
[https://doi.org/10.1007/s10068-016-0234-0]

-
Lejko, D. G. and M. Worek. 2024. Honeydew Honey as a Reservoir of Bacteria with Antibacterial and Probiotic Properties. Antibiotics 13: 855.
[https://doi.org/10.3390/antibiotics13090855]

-
Luca, L., D. Pauliuc and M. Oroian. 2024. Honey microbiota, methods for determining the microbiological composition and the antimicrobial effect of honey-A review Food Chem.: X 23: 101524.
[https://doi.org/10.1016/j.fochx.2024.101524]

-
Ma, J., Q. Lai, F. He, X. Zhang, J. Shui, M. Yu, G. Wei and W. Li. 2023. Microbial source tracking identifies sources of contamination for a river flowing into the yellow sea.
[https://doi.org/10.3389/fmicb.2023.1111297]

-
Meriggi, N., A. Russso, S. Renzi, B. Cerasuolo, M. Nerini, A. Ugolini, M. Marvasi and D. Cavalieri. 2024. Enhancing seafood traceability: tracking the origin of seabass and seabream from the Tuscan coast area by the analysis of the gill bacterial communities. Anim. Microbiome 6(13)
[https://doi.org/10.1186/s42523-024-00300-z]

-
Milla, L., A. Schmidt-Lebuhn, J. Bovill and F. Encinas-Viso. 2023. Monitoring of honey bee floral resources with pollen DNA metabarcoding as a complementary tool to vegetation surveys. Ecol. Solut. Evid. 3: e12120.
[https://doi.org/10.1002/2688-8319.12120]

-
Namin, S. M., M. J. Kim, M. Son and C. Jung. 2022. Honey DNA metabarcoding revealed foraging resource partitioning between Korean native and introduced honey bees (Hymenoptera: Apidae). Sci Rep. 12: 14394.
[https://doi.org/10.1038/s41598-022-18465-5]

- Olaitan P. B., O. E. Adeleke and I. O. Ola. 2007. Honey: a reservoir for microorganisms and an inhibitory agent for microbes. Afr. Health Sci. 7(3):159-165.
-
Rosli, F. N., M. H. F. Hazemi, M. A. Akbar, S. Basir, H. Kassim and H. Bunawan. 2020. Stingless Bee Honey: Evaluating Its Antibacterial Activity and Bacterial Diversity. Insects 11, 500.
[https://doi.org/10.3390/insects11080500]

-
Sabater, C., I. Calvete, X. Vázquez, L. Ruiz, A. Margolles. 2024. Tracing the origin and authenticity of Spanish PDO honey using metagenomics and machine learning. Int. J. Food Microbiol. 421: 110789.
[https://doi.org/10.1016/j.ijfoodmicro.2024.110789]

-
Santorelli, L., T. Wilkinson, R. Abdulmalik, Y. Rai, C. J. Creevey, S. Huws and J. Gutierrez-Merino. 2023. Beehives possess their own distinct microbiomes. Environ. Microbiome 18: 1.
[https://doi.org/10.1186/s40793-023-00460-6]

-
Saravanan, M., G. Mohanapriya, R. Laha and R. Sathishkumar. 2019. DNA barcoding detects floral origin of Indian honey samples. Genome 62: 341-348.
[https://doi.org/10.1139/gen-2018-0058]

-
Scott, T. M., J. B. Rosd, T. M. Jenkins, S. R. Farrah and J. Lulasil. 2002. Microbial Source Tracking: Current Methodology and Future Direction. Appl Environ Microbiol. 68(12): 5796-5803.
[https://doi.org/10.1128/AEM.68.12.5796-5803.2002]

-
Silva, M. S., Y. Rabadzhiev, M. R. Eller, I. Iliev, I. Ivanova, W. and C. Santana. 2017. Microorganisms in honey. Honey analysis, InTech (2017).
[https://doi.org/10.5772/67262]

-
Snowdon, J. A. and D. O. Cliver. 1996. Microorganisms in honey. Int. J. Food Microbiol. 3: 1-26.
[https://doi.org/10.1016/0168-1605(96)00970-1]

-
Soares, S., F. Rodrigues and C. Delerue-Matos. 2023. Towards DNA-Based Methods Analysis for Honey: An Update. Molecules, 28.2106.
[https://doi.org/10.3390/molecules28052106]

-
Ullah, S., F. Huyop, R. A Wahab, N. Huda, H. A. Oyewusi, G. A. Sujana, S. Saloko, A. A. S. P. R. Andriani, M. A. N. Mohamad, A. A. A. Hamid, M. H. M. Nasir, N. S. Antara, I. B. W. Gunam. 2024. The first ITS1 profiling of honey samples from the Southeast Asian region Lombok, Bali and Banggi Island. Sci Rep. 14: 14122.
[https://doi.org/10.1038/s41598-024-64838-3]

-
Vázquez-Quinones, C. R., R. n Moreno-Terrazas, I. Natividad-Bonifacio, E. I. Quinones-Ramírez and C. Vázquez-Salinas. 2018. Microbiological assessment of honey in México Rev Argent Microbiol. 50(1): 75-80.
[https://doi.org/10.1016/j.ram.2017.04.005]

-
Wen, Y., L. Wang, Y. Jin, J. Zhang, L. Su, X. Zhang, J. Zhou and Y. Li. 2017. The Microbial Community Dynamics during the Vitex Honey Ripening Process in the Honeycomb. Front. Microbiol. 29: 8.
[https://doi.org/10.3389/fmicb.2017.01649]

-
Winitzingerode, F. V., U. B.Gobel, E. Stackebrandt. 1997. Determination of microbial diversity in environmental samples: pitfalls of PCR-nbased RNA analysis. FEMS Microbiol. Rev. 21(3): 213-229.
[https://doi.org/10.1111/j.1574-6976.1997.tb00351.x]

-
Wirta, H., N. Abrego, K. Miller, T. Roslin, & E. Vesterinen. 2021. DNA traces the origin of honey by identifying plants, bacteria and fungi. Sci. Rep. 11: 4798.
[https://doi.org/10.1038/s41598-021-84174-0]

-
Xiong, Z. R., J. H. Sogin and R. W. Worobo. 2023. Microbiome analysis of raw honey reveals important factors influencing the bacterial and fungal communities. Front. Microbiol. 13: 1099522.
[https://doi.org/10.3389/fmicb.2022.1099522]