PMA로 자극된 U937 세포에서 프로폴리스와 혼합된 아까시꿀에 의한 대식세포 분화 억제
Abstract
Macrophage differentiation of U937 monocytes is induced by PMA stimulation, which is driven by the expression and phosphorylation of numerous intracellular proteins. We prepared honey, propolis, and a mixture of honey and propolis called Honeypolis, and confirmed the inhibition of macrophage differentiation by PMA. PMA at 10 ng/mL promoted U937 macrophage differentiation, accompanied by increased expression and phosphorylation of TLR4, CK2-α, PPAR-γ, NF-κB, and SOCS3. Furthermore, the U937 cells differentiated into macrophages and became adherent to the culture dish. However, when propolis and Honeypolis were co-treated with PMA, macrophage differentiation was inhibited and cell morphology remained unchanged, and adherent cells were not observed. In addition, propolis and honeypolis were affected the expression and phosphoryaltion of intracellular protein molecules, decreasing the expression of TLR4, CK2-α, SOCS3, and PPAR-γ and the phosphorylation of NF-κB and PPAR-γ. In addition, propolis and honeypolis regulated the major protein of MAPK such as p38 phosphorylation and SAPK/JNK phosphorylation and expression. Especially, honeypolis showed a higher effect on protein expression and phosphorylation than propolis, indicating that the combination of honey and propolis exhibited a synergistic functional effect. In conclusion, our results show that both propolis and honeypolis inhibit PMA-induced U937 macrophage differentiation. And our study suggests that propolis has the immunosuppressive effects, and our results provided in vitro data for immunosuppressive agents application.
Keywords:
Propolis, Honeypolis, U937, Macrophage differenctiaion서 론
단핵구는 대식세포의 주요 전구체로서 (Gautier and Yvan-Charvet, 2014; Strauss et al., 2015), 미생물에 의한 산물, 사이토카인/케모카인 그리고 세포 성장 인자 등을 포함한 환경 자극에 의해 세포의 표현형과 분화 과정이 조절된다 (Bogdan and Nathan, 1993; Lee et al., 1993). 단핵구는 염증 부위에서 모이게 되어 cluster of differentiation 44 (CD44)와 같은 특정 표면 단백질을 통해 extracellular matrix (ECM) 또는 다른 면역 세포에 부착된다 (Geissmann et al., 2010; Ingersoll et al., 2011). 활성화된 단핵구는 분화 프로그램을 통해 빠르게 대식세포로 성숙하는데 이 과정에서 세포 형태 변화, 세포질 복잡성 증가 그리고 lipopolysaccharide co-receptor (CD14), toll-like receptor 2 (TLR2), TLR4 등의 막 단백질의 조절을 특징으로 한다 (Henning et al., 2008; Daigneault et al., 2010; Mantovani et al., 2013; Yoshihara et al., 2013). 반대로 α-integrin M (CD11b), α-integrin X (CD11c), 대식세포에서 발현되는 막 표면 단백질인 CD68 및 당단백질 B7-2 (CD86)은 과발현된다 (Lanier et al., 1995; Ramprasad et al., 1996; Ward et al., 2001; Victoria et al., 2013). 미생물과 T 세포 유래 사이토카인의 자극은 일반적인 대식세포 활성화 및 interleukin-1β (IL-1β), IL-6, IL-13, tumor necrosis factor-α (TNF-α), nitric oxide (NO)와 같은 사이토카인의 생성으로 이어진다 (Brune et al., 2013). 이 과정에서 대식세포는 환경 조건에 따라 다른 표현형 특성을 획득하여 기능적 다양성을 가지게 된다 (Gordon and Taylor, 2005). 대식세포가 활성화되는 동안 nicotinamide adenine dinucleotide phosphate (NADPH) 산화효소로부터 생성되는 reactive oxygen species (ROS)는 병원균의 제거를 돕고 염증 반응에 대한 신호 전달 네트워크에서 중요한 구성 요소가 된다 (Gordon and Tayor, 2005; Lawrence and Natoli, 2011; Brune et al., 2013).
그러나 조직에서 분리된 일차 배양 대식세포는 표현형이 매우 이질적이고, 일단 분화된 세포는 조직 항상성 유지 및 침입하는 미생물에 대한 방어를 포함한 특수 목적에 맞는 기능을 발달시킨다 (Mosser and Edwards, 2009). 또한, 대식세포는 선천 면역 반응을 매개하고 적응 면역 반응에 참여한다 (Saric et al., 2015; Celhar et al., 2016). 그러나 일차 조직 배양을 통해 획득된 대식세포 및 단핵구는 분리 후 증식에 어려움이 있다. 이들의 분리를 위해서는 침습적 시술을 통해 특정 조직에서 채취해야 하고, 실험을 위해 사용할 수 있는 세포의 수가 매우 적기 때문에 일차 배양 대식세포는 연구 사용에 매우 제한적이 된다 (Schwende et al., 1996). 이러한 이유로 대식세포 분화 연구는 세포 활용의 한계로 인해 U937 또는 THP-1과 같은 세포를 단핵구 세포 분화 모델로 많이 사용된다. 특히 U937 세포주는 단핵구의 특성을 지닌 림프종에서 유래되었으며 (Sundström et al., 1976; Harris and Ralph, 1985; Liu et al., 1996), phorbol 12-myristate 13-acetate (PMA), 25-dihydroxyvitamin D3 (VD3), interferon 및 retinoic acid 등의 자극에 따라 다양한 대식세포로 분화된다 (Hattori et al., 1983; Olsson et al., 1983; Kiley and Parker, 1995; Moriuchi et al., 1998; Naldini et al., 1998; Song et al., 2015). 이 중 PMA에 의한 자극은 protein kinase C (PKC)의 강력한 활성제인 diacylglycerol (DAG)의 유사체이므로, PMA 처리 시 U937 세포에서는 PKC 신호 전달 경로가 자극되어 nuclear factor kappa-light-chain-enhancer of activated B cells (NF-κB) 및 activator protein-1 (AP-1)을 포함한 여러 전사 인자를 통해 광범위한 유전자 발현이 변화된다 (Chiu et al., 1987; Ghosh and Baltimore, 1990; Pedrinaci et al., 1990; Fan et al., 2014). 특히, NF-κB 단백질은 염증성 사이토카인 발현에 중요한 인자가 되는데 (Li and Verma, 2002), NF-κB의 전사 활성은 주로 IκB kinase (IKK)의 기질인 세포성 억제 단백질 IκB에 의해 조절된다 (Baeuerle and Baltimore, 1998). 또한 mitogen activated protein kinase (MAPK)와 같은 다양한 신호전달 경로 역시 활성화되어 대식세포 분화에 영향을 끼친다 (Lee et al., 1997; Chen and Lin, 2001).
프로폴리스는 식물에서 유래된 다양한 물질을 꿀벌이 타액을 혼합하여 만든 것으로, 수많은 기능성 물질을 포함하고 있다. 본래 프로폴리스는 꿀벌이 벌집을 보호하기 위한 수단이나 벌집의 손상된 부분을 수리하는 목적으로 활용되었다 (Burdock, 1998). 고대부터 인류 역시 프로폴리스를 상처 회복을 위한 목적으로 활용하였는데, 현재는 프로폴리스에 수많은 기능성 물질이 포함된 것을 이용하여 다양한 분야에 활용하고 있다 (Fernandes Junior et al., 2005; Sforcin, 2007). 프로폴리스는 매우 다양하고도 풍부한 플라보노이드와 폴리페놀을 함유하고 있기 때문에 항균, 항산화 그리고 항염증 작용에 주로 이용되어져 왔다. 그러나 최근 Yeh 등은 플라보노이드의 인지 기능 개선 효과에 대해 보고하였고 (Yeh et al., 2021), Kim 등은 프로폴리스가 알츠하이머의 원인이 되는 tau 단백질의 과인산화를 해소할 수 있음을 보고하였다 (Kim et al., 2021). 또한 Kim 등은 MPTP에 의한 α-synuclein 단백질의 이상 응집을 프로폴리스가 해소할 수 있음을 밝혀, 프로폴리스의 파킨슨 질병 억제 가능성을 보고하였다 (Kim et al., 2022). 이와 같이 프로폴리스의 기능성 효과를 이용한 활용 범위가 점차 확대되고 있다.
이에 본 연구에서는 프로폴리스의 U937의 분화 억제에 대한 효과를 구명하여 면역억제제로서 프로폴리스를 활용하는 것에 대한 기초 연구 자료를 제공하고자 한다. U937 단핵구 세포를 이용하여 프로폴리스의 대식세포 분화 억제를 확인하였고, 프로폴리스와 꿀이 혼합된 허니폴리스를 이용하여 대식세포 분화 억제에 대한 기능성 상승 효과를 함께 검증하였다. 그러나 프로폴리스가 단핵구의 대식세포 분화 억제에 대한 기전 연구는 아직 미비한 상태로서 앞으로 추가적으로 연구를 통해 입증해야 할 것 이다.
재료 및 방법
1. 허니폴리스 제작
허니폴리스 제작을 위해 사용된 아까시꿀과 프로폴리스 추출물은 국내 양봉농협에서 판매하고 있는 총 플라보노이드 함량 10 mg/mL를 기준으로 하는 제품을 사용하였다. 꿀 2.5 g을 80% 에탄올과 1 : 1의 비율로 혼합하여, vortex mixter와 rotator를 이용하여 완전히 혼합하였다. 여기에 다시 동량의 3차 증류수를 첨가하고, 250 μL의 프로폴리스 추출물을 첨가하고 완전히 혼합한 다음, 0.45 μm의 syringe filter를 이용하여 필터링하였다. 프로폴리스 추출물과 꿀의 혼합비는 1 : 10이며, 제작된 시료는 사용하기까지 냉장 보관하였다.
2. Media & Reagents
세포 배양에 사용된 배지는 Gibco* (Gaithersburg, MD, USA)사의 RPMI1640 배지를 사용하였으며, 미생물 성장 억제를 위해 Gibco사의 100× anti-anti를 최종 1×의 농도로 배지에 첨가하였다. Fetal bovine serum (FBS)는 Gibco사의 Heat inactivated FBS를 구입하여 세포 배양 배지의 1/10 부피로 첨가하였다. 대식세포 분화를 위한 PMA는 Sigma-Aldrich (St Louis, MO, USA)에서 구입하였으며, Western blotting에 사용된 1차 항체 중 CK2-α, SOCS3, PPAR-γ, phospho-p38, total p38, phospho-SAPK/JNK 그리고 total SAPK/JNK는 Cell Signaling Technology (Berkeley, CA, USA)에서 구입하였으며, TLR4, NF-κB 그리고 GAPDH는 Santacruz Biotechnology (Dallas, TX, USA)에서 구입하여 사용하였다.
3. 세포주 배양 및 프로폴리스의 대식세포 분화 억제
실험에 사용된 U937 단핵구 세포주는 한국세포주은행에서 구입하여 계대배양하여 사용하였다. U937 세포주는 세포 배양액에 suspension되어 자라기 때문에 20 mL의 배지를 사용하고, 세포 배양 조건은 37°C에서 5%의 CO2를 공급하면서 배양하였다.
프로폴리스와 허니폴리스의 U937 세포주 대식세포 분화 억제를 확인하고자 하였다. 대식세포 분화는 U937 세포주에 10 ng/mL의 PMA를 처리하여 유도하였으며, 프로폴리스 및 허니폴리스의 대식세포 분화 억제를 확인하기 위해 아까시꿀, 프로폴리스 그리고 허니폴리스를 각각 10 ng/mL의 PMA와 함께 세포에 처리하였다. 세포에 처리된 프로폴리스의 농도는 25 μg/mL로 설정하였다. 각 시약을 처리하고 24시간 동안 배양하고, 다음 날 EVOS XL Core (U.S.A.) 현미경으로 세포 형태를 촬영하였다. 실험 처리 조건을 다음 표에 요약하였다.
4. 세포 단백질 추출 및 정량
세포 형태를 촬영하고 각 실험구의 세포에서 단백질을 추출하였다. U937 세포는 배양 접시에 부착되지 않고 배지에 부유된 상태로 성장하지만, PMA에 의해 분화가 일어나면 세포는 배양 접시 바닥에 부착된다. 따라서 세포에 처리된 조건에 따라 단백질 추출법이 달라지게 된다. 현미경으로 세포를 확인하고 부착된 세포의 경우 배지를 제거하고 1× phosphate buffered saline (PBS) 용액으로 1회 수세한 뒤, 200 μL의 Nonidet P-40 (NP-40) cell lysis 용액을 첨가하여 cell scraper로 세포를 용해하였다. 부유된 세포는 50 mL conical tube에 모아서 3,000 rpm에서 15분간 원심분리한 다음, 배양액을 제거하고 10 mL의 1× PBS를 첨가하여 수세하고 200 μL의 NP-40 cell lysis 용액을 첨가하고, vortex mixer로 강하게 교반하여 단백질을 추출하였다. 추출된 단백질은 bicinchronic acid (BCA) 단백질 정량법으로 정량하였다. 정량된 단백질에 5× SDS sample buffer (250 mM Tris-HCl (pH 6.8), 5% 2-Mercaptoethanol, 10% SDS, 0.5% Bromophenol blue, 50% Glycerol)를 첨가하고 100°C에서 10분간 boiling하여 단백질을 변성시켰다. 준비된 단백질 시료 20 μg을 Western blotting에 사용하였다.
5. Western blotting
정량된 단백질 20 μg을 4~15% TGX gradient gel [Bio-Rad (Hercules, CA, USA)]에 loading하고, 100 voltage에서 1시간 동안 단백질을 분자량에 따라 분획하였다. Gel 내의 단백질을 transblot (Bio-Rad)을 이용하여 15 voltage에서 5분간 polyvinylidene fluoride (PVDF) membrane에 transfer하였다. 단백질이 전이된 membrane을 1× tris-buffered saline-tween 20 (TBS-T) 용액에 1회 수세한 뒤, 항체의 비특이적 반응 차단을 위해 0.02%의 sodium azide (Sigma)가 첨가된 2% non-fat dry milk (Bio-Rad) 용액에 실온에서 1시간 동안 반응시켰다. 이후 표적 단백질 검출을 위해 인산화 항체는 1 : 500으로 희석하고, 그 외 다른 1차 항체는 1 : 1,000의 희석배율로 실온에서 20시간 동안 반응시켰다. 이후, membrane을 1× TBS-T 용액으로 수세한 뒤, 1차 항체의 source에 따라 2차 항체인 goat anti-mouse-HRP 또는 goat anti-rabbit-HRP를 1 : 2,000의 배율로 5% non-fat dry milk (without sodium aizde)에 희석하여 실온에서 2시간 동안 반응시켰다. Membrane을 1× TBS-T로 5회 수세한 뒤, GenDEPOT (Baker, TX, USA) 사의 ECL pico detection system으로 발색한 다음, ChemiDOC (Bio-Rad)으로 표적 단백질을 검출하였다.
결과 및 고찰
1. 프로폴리스와 허니폴리스에 의한 단핵구의 대식세포 분화 억제
Fig. 1에는 PMA로 자극되어 대식세포로 분화된 U937 세포와 프로폴리스와 허니폴리스에 의해 분화가 억제된 세포의 형태를 보여주고 있다. PMA로 자극되지 않은 U937 세포는 배지에서 부유하면서 둥근 형태의 세포 형태를 띠고 있지만, PMA로 자극된 경우 세포는 대식세포로 분화되어 세포 형태도 둥근형태가 아닌 뚜렷한 핵의 모습이 나타나고 바닥에 부착된 형태로 바뀌게 된다. 그러나 꿀, 프로폴리스 그리고 허니폴리스를 U937 세포에 처리했을 때는 정상군과 똑같은 형태를 띠고 있다. PMA와 꿀을 세포에 처리한 경우, 꿀은 PMA의 효과를 억제하지 못하며 PMA 단독 처리와 마찬가지로 세포가 분화된 형태로 나타났다. PMA와 프로폴리스, PMA와 허니폴리스를 처리한 경우에는 정상군과 같은 둥근 형태의 세포로 존재하였으며, 이는 프로폴리스가 PMA의 세포 자극을 차단하여 세포 분화를 억제한 것을 보여주고 있다. PMA의 용매 대조군으로 사용된 DMSO를 처리한 실험구와 꿀, 프로폴리스, 허니폴리스의 용매 대조군으로 사용된 에탄올에서는 세포의 형태가 정상군과 동일한 것으로 나타났으며, 이는 대식세포 분화 관련 기전이 PMA, 프로폴리스 그리고 허니폴리스 등에 의해서 나타난 영향임을 의미한다.
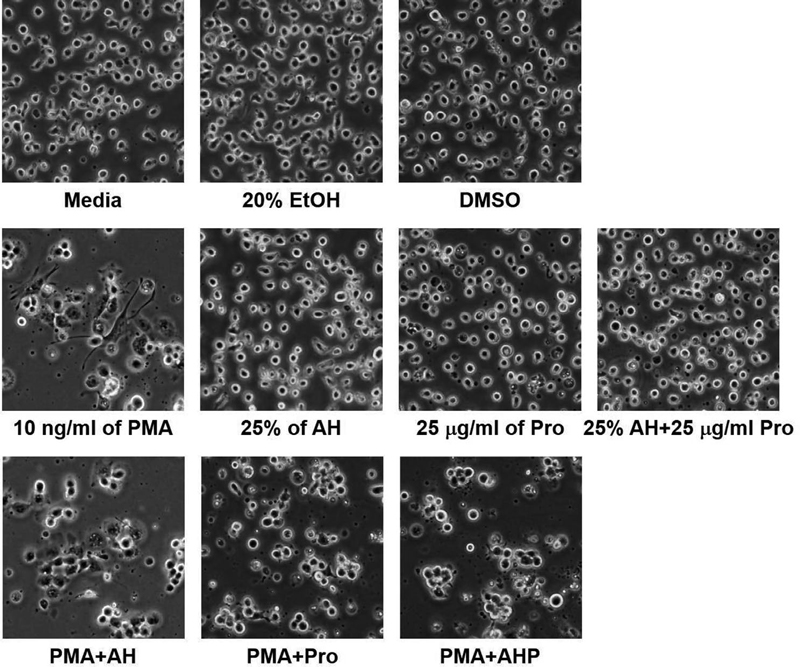
Change of the U937 cell morphology by PMA, Robinia honey, propolis and honeypolis. Cells were treated with PMA (10 ng/mL), AH (50 μL), Pro (25 μg/mL), AHP (25 μg/mL including propolis), PMA+AH, PMA+Pro and PMA+AHP for 24 hrs, respectively. 20% EtOH and DMSO is solvent control (AH: Robinia honey, Pro: Propolis, AHP: Robinia honey+propolis mix).
2. 세포 내 단백질 마커 발현을 통한 프로폴리스의 분화 억제
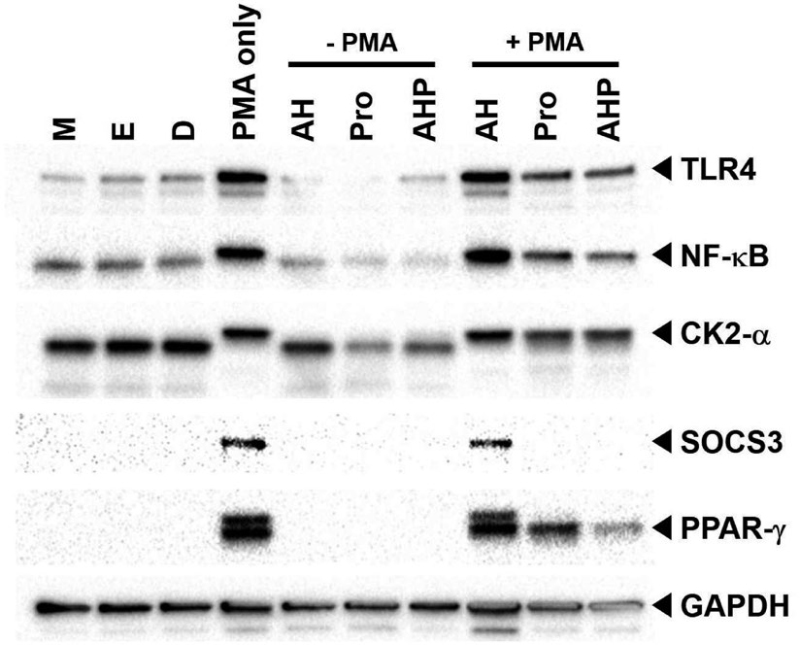
Fig. 2에는 대식세포 내에서 발현되는 단백질을 이용하여 프로폴리스의 대식세포 분화 억제 효과 그리고 허니폴리스에 의한 분화 억제 기능성 상승 효과를 나타내고 있다. 세포 내 다양한 단백질 중 대식세포에서 특이적으로 과발현되거나 활성화되는 단백질을 표적 마커로 선정하여 Western blotting을 통해 발현 차이를 확인하였다. 단핵구 세포에서 대식세포로 분화될 때 발현양이 증가하는 대표적인 마커 단백질은 TLR4, PPAR-γ 등이 존재하며, 단백질의 인산화 증가를 통해 확인할 수 있는 마커 단백질은 NF-κB, CK2-α, PPAR-γ 등이 있다. 본 논문에서는 일반적으로 알려진 마커 단백질 이외에 SOCS3 단백질의 발현 역시 대식세포 분화에 관련된 마커 단백질임을 추가로 제시하고자 한다. TLR4, SOCS3 그리고 PPAR-γ는 PMA로 세포가 자극되면 발현양이 증가되며, NF-κB, CK2-α 그리고 PPAR-γ는 인산화가 증가된다. PMA와 함께 꿀을 처리했을 경우에는 분화 억제 효과가 나타나지 않고 PMA 처리한 실험구와 차이가 없었다. 그러나 프로폴리스와 허니폴리스를 PMA와 함께 처리할 경우 TLR4, PPAR-γ 그리고 SOCS3의 단백질이 정상군과 마찬가지의 수준으로 발현이 감소되었다. 또한 NF-κB, CK2-α 그리고 PPAR-γ의 인산화 역시 감소된 것으로 나타났다. 특히. NF-κB의 인산화와 PPAR-γ의 발현과 인산화에 있어 기능성 효과는 프로폴리스를 사용한 것보다 허니폴리스에서 더 강한 효과를 나타냈다. 이는 꿀과 프로폴리스가 혼합되면서 대식세포 분화 억제에 대한 기능성 상승효과를 나타내고 있다. GAPDH는 본 실험에서 사용된 정량 대조군이다.
3. 프로폴리스와 허니폴리스에 의한 MAPK의 신호 경로 조절
단핵구 세포로 존재하는 U937 세포가 PMA로 자극되어 대식세포로 분화될 때 나타나는 MAPK의 신호 경로 관련 단백질의 인산화와 발현을 확인하였다. MAPK 경로에서 대표되는 p38과 SAPK/JNK의 인산화와 발현을 확인한 결과를 Fig. 3에서 보여주고 있다. p38의 경우 대식세포로 분화될 때 단백질의 발현양에서는 차이가 나타나지 않았다. 또한 꿀, 프로폴리스 그리고 허니폴리스에 의해서도 단백질 발현에는 영향이 나타나지 않았다. 그러나 PMA, 꿀, 프로폴리스 그리고 허니폴리스에 의해서 p38의 인산화가 조절됨이 나타났다. PMA 처리에 의해 p38의 인산화가 감소되었고, 프로폴리스와 허니폴리스에 의해 인산화가 다시 증가됨이 나타났다. 그러나 PMA가 처리되지 않은 상태에서도 프로폴리스와 허니폴리스는 p38의 인산화를 증가시켰는데, 이는 이들이 세포의 MAPK 경로 중 p38의 조절에 직접 관여하고 있음을 의미한다.
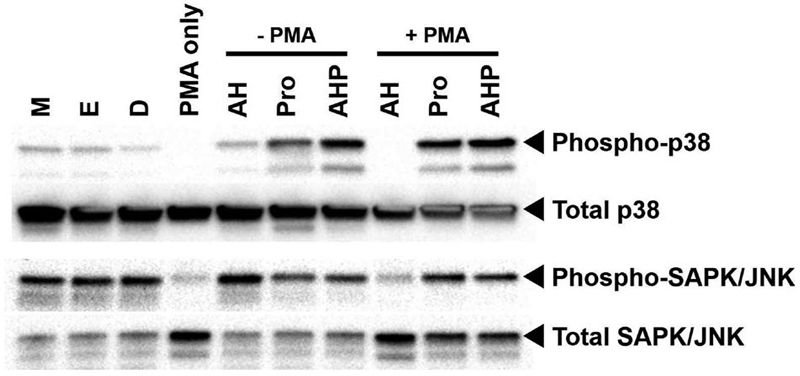
Propolis and honeypolis regulated MAPK kinase phosphorylation and its expression. 20 μg of proteins were used in each experiment groups and seperated in 4~15 gradient gel. Phosphorylation antibody of p38 and SAPK/JNK were diluted at 1 : 500. And total p38 and SAPK/JNK antibodies were diluted at 1 : 1,000. Antibody incubation for overnight at R.T.
반면 MAPK 중의 SAPK/JNK는 다른 양상으로 나타났다. PMA에 의해서 이들의 인산화가 감소되었는데, 프로폴리스와 허니폴리스는 p38과는 달리 이 단백질의 인산화에 직접적으로 관여하지 않았다. 그러나 PMA와 함께 처리되었을 때는 PMA에 의한 인산화 감소를 프로폴리스와 허니폴리스가 차단하고 있음을 알 수 있다. 또한 SAPK/JNK는 단백질 발현에 있어서도 차이를 나타냈음을 알 수 있다. PMA에 의해 SAPK/JNK의 단백질이 강하게 발현됨을 알 수 있는데, 프로폴리스와 허니폴리스에 의해 단백질 발현이 감소되는 것으로 나타났다.
고 찰
단핵구는 세포 외부의 자극이나 환경 변화에 의해 대식세포로 분화하며, 이는 체내 면역 방어에 핵심적인 역할을 담당한다. 그러나 병원체의 침투나 지속적인 염증 자극으로 인해 과도한 면역 반응이 유발될 수 있으며, 장기이식 과정에서도 이식 거부 반응으로 자가 면역 질환이 발생하여 면역억제제 사용이 필수적이다 (De Bleser et al., 2009). 최근 코로나 팬더믹에서도 사이토카인 폭풍에 의한 과면역 반응 문제가 크게 부각된 바 있다 (Sun et al., 2020).
본 연구에서는 대표적인 양봉산물인 꿀과 프로폴리스를 활용하여 과면역 억제 가능성을 탐색하고, 단핵구의 대식세포 분화 과정을 억제할 수 있는 기능성을 분자 수준에서 검증하였다. 이전의 연구에서도 단핵구의 대식세포 분화 과정에서 carbon monoxide (CO)의 분화 저해 효과 및 관련 단백질인 HO-1, CD14, CD18, ICAM-1 등의 발현을 확인하였지만 (Kim et al., 2017), 본 논문에서는 건강기능식품으로 손쉽게 활용할 수 있는 양봉산물을 활용하여 대식세포 분화에 관여하는 단백질과 세포 내 신호 전달 기전에 대한 단백질 발현 및 기능 변화를 확인하 였다.
PMA 자극에 의해 U937 단핵구 세포의 대식세포 분화가 유도되며, 이 과정은 TLR4, NF-κB, CK2-α, PPAR-γ 등의 단백질 발현 및 인산화와 연관됨을 확인하였다. 프로폴리스와 허니폴리스는 PMA에 유발되는 이들 단백질의 발현 증가와 인산화를 억제하였으며, 특히 허니폴리스가 더 강력한 억제효과를 나타내었다. 또한 기존의 보고되지 않았던 새로운 대식세포 분화 마커인 SOCS3의 발현증가가 PMA 처리에 의해 유도됨을 확인하였고, 프로폴리스 및 허니폴리스가 이를 억제함을 규명하였다. 이는 단핵구의 대식세포 분화에 새로운 단백질이 관여함을 제시하며, 향후 면역세포 분화의 세포 신호 네트워크를 규명하는 연구로 확장될 수 있음을 시사한다. 추가적으로 MAPK 신호 경로 역시 대식세포 분화에 관여하며, 프로폴리스와 허니폴리스가 해당 경로 단백질의 인산화를 조절함을 확인하였다. 이 과정은 여러 세포 내 단백질에 직간접적으로 영향을 미치는 것으로 나타났다.
본 연구 결과, 프로폴리스 추출물 단독으로 처리한 것보다 아까시꿀과 프로폴리스를 혼합하여 제작한 제형인 허니폴리스가 기능성 효과 면에서 우수함을 입증하였는데, 이는 양봉산물 혼합에 의한 기능성 상승효과를 나타냄을 제시하는 것이다. 또한 프로폴리스는 다양한 생리활성 물질을 함유하고 있으므로 향후 성분 동정을 통해 과면역 반응 및 대식세포 분화 억제에 기여하는 핵심 물질을 규명하고 표준화하는 연구가 필요하다. 또한 본 연구에서 제시하는 결과는 in vitro에서 나타난 결과만을 밝혔는데, 앞으로 in vivo에서의 추가적인 연구가 반드시 필요하다. 본 연구는 프로폴리스와 허니폴리스의 면역 조절 기능을 새롭게 밝혔으며, 국내 양봉산물의 기능성 근거를 확립하고 소비 촉진에 기여할 수 있을 것으로 기대된다.
Acknowledgments
본 연구는 농촌진흥청 어젠다연구사업 (과제번호:RS-2021-RD010155)에 의해 수행되었습니다.
References
-
Baeuerle, P. A. and D. Baltimore. 1988. I kappa B: a specific inhibitor of the NF-kappa B transcription factor. Science. 242: 540-546.
[https://doi.org/10.1126/science.3140380]

-
Bogdan, C. and C. Nathan. 1993. Modulation of macrophage function by transforming growth factor p, interleukin-4, and interleukin-10. Ann. N. Y. Acad. Sci. 685: 713-739.
[https://doi.org/10.1111/j.1749-6632.1993.tb35934.x]

-
Burdock, G. A. 1998. Review of the biological properties and toxicity of bee propolis (propolis), Food Chem. Toxicol. 36: 347-363.
[https://doi.org/10.1016/S0278-6915(97)00145-2]

-
Brune, B., N. Dehne, N. Grossmann, M. Jung, D. Namgaladze, T. Schmid, A. Knethen and A. Weigert. 2013. Redox control of inflammation in macrophages. Antioxidants & Redox Signaling 19: 595-637.
[https://doi.org/10.1089/ars.2012.4785]

-
Celhar, T., S. Pereira-Lopes, S. I. Thornhill, H. Y. Lee, M. K. Dhillon, M. Poidinger, C. John, L. Lim, S. Biswas and A.-M. Fairhurst. 2016. TLR7 and TLR9 ligands regulate antigen presentation by macrophages. Int. Immunol. 28: 223-232.
[https://doi.org/10.1093/intimm/dxv066]

-
Chen, B. C. and W. W. Lin. 2001. PKC- and ERK-dependent activation of I kappa B kinase by lipopolysaccharide in macrophages: enhancement by P2Y receptor-mediated CaMK activation. British J. Pharmacol. 134: 1055-1065.
[https://doi.org/10.1038/sj.bjp.0704334]

-
Chiu, R., M. Imagawa, R. J. Imbra, J. R. Bockoven and M. Karin. 1987. Multiple cis- and trans-acting elements mediate the transcriptional response to phorbol esters. Nature 329: 648-651.
[https://doi.org/10.1038/329648a0]

-
Daigneault, M., J. A. Preston, H. M. Marriott, M. K. B. Whyte and D. H. Dockrell. 2010. The identification of markers of macrophage differentiation in PMA-stimulated THP-1 cells and monocyte-derived macrophages. PLoS One 5: e8668.
[https://doi.org/10.1371/journal.pone.0008668]

-
De Bleser L, M. Matteson, F. Dobbels, C. Russell and De Geest S. 2009. Interventions to improve medication-adherence after transplantation: a systematic review. Transplant International 22: 780-797.
[https://doi.org/10.1111/j.1432-2277.2009.00881.x]

-
Fan, H. C., C. Fernandez-Hernando and J. H. Lai. 2014. Protein kinase C isoforms in atherosclerosis: pro- or anti-inflammatory? Biochem. Pharmacol. 88: 139-149.
[https://doi.org/10.1016/j.bcp.2014.01.006]

-
Fernandes Junior, A., E. C. Balestrin, J. E. Betoni, O. Orsi Rde, L. da Cunha Mde and A. C. Montelli. 2005. Propolis: anti-Staphylococcus aureus activity and synergism with antimicrobial drugs. Mem. Inst. Oswaldo Cruz. 100: 563-566.
[https://doi.org/10.1590/S0074-02762005000500018]

-
Gautier, E. L. and L. Yvan-Charvet. 2014. Understanding macrophage diversity at the ontogenic and transcriptomic levels. Immunol. Rev. 262: 85-95.
[https://doi.org/10.1111/imr.12231]

-
Geissmann, F., M. G. Manz, S. Jung, M. H. Sieweke, M. Merad and K. Ley. 2010. Development of monocytes, macrophages, and dendritic cells. Science 327: 656-661.
[https://doi.org/10.1126/science.1178331]

-
Ghosh, S. and D. Baltimore. 1990. Activation in vitro of NF-kappa B by phosphorylation of its inhibitor I kappa B. Nature 344: 678-682.
[https://doi.org/10.1038/344678a0]

-
Gordon, S. and P. R. Taylor. 2005. Monocyte and macrophage heterogeneity. Nature Reviews Immunology 5: 953-964.
[https://doi.org/10.1038/nri1733]

-
Harris, P. and P. Ralph. 1985. Human leukemic models of myelomonocytic development: a review of the HL-60 and U937 cell lines. J. Leukoc. Biol. 37: 407-422.
[https://doi.org/10.1002/jlb.37.4.407]

-
Hattori, T., M. Pack, P. Bougnoux, Z. L. Chang and T. Hoffman. 1983. Interferon-induced differentiation of U937 cells. Comparison with other agents that promote differentiation of human myeloid or monocyte-like cell lines. J. Clin. Invest. 72: 237-244.
[https://doi.org/10.1172/JCI110962]

-
Henning, L. N., A. K. Azad, K. V. L. Parsa, J. E. Crowther, S. Tridandapani and L. S. Schlesinger. 2008. Pulmonary surfactant protein A regulates TLR expression and activity in human macrophages. J. Immunol. 180: 7847-7858.
[https://doi.org/10.4049/jimmunol.180.12.7847]

-
Ingersoll, M. A., A. M. Platt, S. Potteaux and G. J. Randolph. 2011. Monocyte trafficking in acute and chronic inflammation. Trends in Immunology 32: 470-477.
[https://doi.org/10.1016/j.it.2011.05.001]

-
Kiley, S. C. and P. J. Parker. 1995. Differential localization of protein kinase C isozymes in U937 cells: evidence for distinct isozyme functions during monocyte differentiation. J. Cell Sci. 108: 1003-1016.
[https://doi.org/10.1242/jcs.108.3.1003]

-
Kim, D. S., M. S. Lee, H. S. Kim, H. Y. Lee, O. Y. Kim, Y. R. Kang and D. H. Sohn. 2017. Carbon monoxide inhibits PMA-induced differentiation in human monocytic. J. Life Sci. 27: 217-224.
[https://doi.org/10.5352/JLS.2017.27.2.217]

-
Kim, S.-K., H. Y. Kim, S. G. Kim, S. M. Han, S. Ryu and S. O. Woo. 2022. The effect of Korean propolis for apoptosis by MPTP-mediated Parkinson’s disease and its molecular mechanism in SH-SY5Y neuroblastoma cells. J. Apic. 37: 83-90.
[https://doi.org/10.17519/apiculture.2022.04.37.1.83]

-
Kim, S.-K., S. M. Han, S. G. Kim, H. Y. Kim, S. Ryu and S. O. Woo. 2021. Inhibition of tau hyperphosphorylation and its molecular mechanism by Korean propolis extracts. J. Apic. 36: 169-176.
[https://doi.org/10.17519/apiculture.2021.09.36.3.169]

-
Lanier, L. L., S. O’Fallon, C. Somoza, J. H. Phillips, P. S. Linsley, K. Okumura, D. Ito and M. Azuma. 1995. CD80 (B7) and CD86 (B70) provide similar costimulatory signals for T cell proliferation, cytokine production, and generation of CTL. J. Immunol. 154: 97-105.
[https://doi.org/10.4049/jimmunol.154.1.97]

-
Lawrence, T. and G. Natoli. 2011. Transcriptional regulation of macrophage polarization: enabling diversity with identity. Nature Reviews Immunology 11: 750-761.
[https://doi.org/10.1038/nri3088]

-
Lee, F. S., J. Hagler, Z. J. Chen and T. Maniatis. 1997. Activation of the IkappaB alpha kinase complex by MEKK1, a kinase of the JNK pathway. Cell. 88: 213-222.
[https://doi.org/10.1016/S0092-8674(00)81842-5]

-
Lee, S. C., W. Liu, P. Roth, D. W. Dickson, J. W. Berman and C. F. Brosnan. 1993. Macrophage colony-stimulating factor in human fetal astrocytes and microglia. Differential regulation by cytokines and lipopolysaccharide, and modulation of class II MHC on microglia. J. Immunol. 150: 594-604.
[https://doi.org/10.4049/jimmunol.150.2.594]

-
Li, Q. and I. M. Verma. 2002. NF-kappaB regulation in the immune system. Nature Rev. Immuno. 2: 725-734.
[https://doi.org/10.1038/nri910]

-
Liu, M., M. H. Lee, M. Cohen, M. Bommakanti and L. P. Freedman. 1996. Transcriptional activation of the Cdk inhibitor p21 by vitamin D3 leads to the induced differentiation of the myelomonocytic cell line U937. Genes Dev. 10: 142-153.
[https://doi.org/10.1101/gad.10.2.142]

-
Mantovani, A., S. K. Biswas, M. R. Galdiero, A. Sica and M. Locati. 2013. Macrophage plasticity and polarization in tissue repair and remodelling. J. Pathol. 229: 176-185.
[https://doi.org/10.1002/path.4133]

-
Moriuchi, H., M. Moriuchi and A. S. Fauci. 1998. Differentiation of promonocytic U937 subclones into macrophage-like phenotypes regulates a cellular factor (s) which modulates fusion/entry of macrophagetropic human immunodeficiency virus type 1. J. Virol. 72: 3394-3400.
[https://doi.org/10.1128/JVI.72.4.3394-3400.1998]

-
Mosser, D. M. and J. P. Edwards. 2009. Exploring the full spectrum of macrophage activation. Genetics 958-969.
[https://doi.org/10.1038/nri2448]

-
Naldini, A., L. Sower, V. Bocci, B. Meyers and D. H. Carney. 1998. Thrombin receptor expression and responsiveness of human monocytic cells to thrombin is linked to interferon-induced cellular differentiation. J. Cell. Physio. 177: 76-84.
[https://doi.org/10.1002/(SICI)1097-4652(199810)177:1<76::AID-JCP8>3.3.CO;2-0]

- Olsson, I., U. Gullberg, I. Ivhed and K. Nilsson. 1983. Induction of differentiation of the human histiocytic lymphoma cell line U-937 by 1 alpha, 25-dihydroxycholecalciferol. Cancer Res. 43: 5862-5867.
-
Pedrinaci, S., F. Ruiz-Cabello, O. Gomez, A. Collado and F. Garrido. 1990. Protein kinase C-mediated regulation of the expression of CD14 and CD11/CD18 in U937 cells. Int. J. Cancer J. Int. du Cancer. 45: 294-298.
[https://doi.org/10.1002/ijc.2910450215]

-
Ramprasad, M. P., V. Terpstra, N. Kondratenko, O. Quehenberger and D. Steinberg. 1996. Cell surface expression of mouse macrosialin and human CD68 and their role as macrophage receptors for oxidized low density lipoprotein. Proc. Natl. Acad. Sci. USA. 93: 14833-14838.
[https://doi.org/10.1073/pnas.93.25.14833]

-
Saric, A., V. E. B. Hipolito, J. G. Kay, J. Canton, C. N. Antonescu and R. J. Botelho. 2015. mTOR controls lysosome tubulation and antigen presentation in macrophages and dendritic cells. Mol. Biol. Cell. 27: 321-333.
[https://doi.org/10.1091/mbc.e15-05-0272]

-
Schwende, H., E. Fitzke, P. Ambs and P. Dieter. 1996. Differences in the state of differentiation of THP-1 cells induced by phorbol ester and 1,25-dihydroxyvitamin D3. J. Leukoc. Biol. 59: 555-561.
[https://doi.org/10.1002/jlb.59.4.555]

-
Sforcin, J. M. 2007. Propolis and the immune system: a review. J. Ethnopharmacol. 113: 1-14.
[https://doi.org/10.1016/j.jep.2007.05.012]

-
Song, M. G., I. G. Ryoo, H. Y. Choi, B. H. Choi, S. T. Kim, T. H. Heo, J. Y. Lee, P. H. Park and M. K. Kwak. 2015. NRF2 signaling negatively regulates phorbol-12-myristate-13-acetate (PMA)-induced differentiation of human monocytic U937 cells into pro-inflammatory macrophages. PLoS One 10: e0134235.
[https://doi.org/10.1371/journal.pone.0134235]

-
Strauss, O., P. R. Dunbar, A. Bartlett and A. Phillips. 2015. The immunophenotype of antigen presenting cells of the mononuclear phagocyte system in normal human liver - A systematic review. J. Hepatol. 62: 458-468.
[https://doi.org/10.1016/j.jhep.2014.10.006]

-
Sun, X., T. Wang, D. Cai, Z. Hu, J. Chen, H. Liao, L. Zhi, H. Wei, Z. Zhang, Y. Qiu, J. Wang and A. Wang. 2020. Cytokine storm intervention in the early stages of COVID-19 pneumonia. Cytokine Growth Factor Rev. 53: 38-42.
[https://doi.org/10.1016/j.cytogfr.2020.04.002]

-
Sundstrom, C. and K. Nilsson. 1976. Establishment and characterization of a human histiocytic lymphoma cell line (U-937). Int. J. Cancer. 17: 565-577.
[https://doi.org/10.1002/ijc.2910170504]

-
Victoria, S., J. R. Temerozo, L. Gobbo, H. K. Pimenta-Inada and D. C. Bou-Habib. 2013. Activation of Toll-like receptor 2 increases macrophage resistance to HIV-1 infection. Immunobiology 218: 1529-1536.
[https://doi.org/10.1016/j.imbio.2013.06.006]

-
Ward, J. O., M. J. Mcconnell, G. W. Carlile, P. P. Pandolfi, J. D. Licht and L. P. Freedman. 2001. The acute promyelocytic leukemia-associated protein, promyelocytic leukemia zinc finger, regulates 1, 25-dihydroxyvitamin D 3-induced monocytic differentiation of U937 cells through a physical interaction with vitamin D3 receptor. Blood. 98: 3290-3300.
[https://doi.org/10.1182/blood.V98.12.3290]

-
Yeh, T.-S., C. Yuan, A. Ascherio, B. Rosner, W. Willett and D. Blacker. 2021. Long-term dietary flavonoid intake and subjective congnitive decline in US men and women. Neurology 97: e1041-e1056.
[https://doi.org/10.1212/WNL.0000000000012454]

- Yoshihara, E., S. Masaki, Y. Matsuo, Z. Chen, H. Tian and J. Yodoi. 2013. From monocytes to M1/M2 macrophages: phenotypical vs. functional differentiation. Front Immunol. 4: 1-22.